Vírus têm sido frequentemente identificados em diversas neoplasias humanas, embora seu papel etiológico em alguns tumores ainda seja motivo de controvérsia. Os principais vírus com capacidade oncogênica são os poliomavírus, especificamente o poliomavírus de células de Merkel (MCPyV). Revisões recentes na taxonomia dos poliomavírus dividiram a família Polyomaviridae em seis gêneros, incluindo 117 espécies, com um total de 14 espécies que infectam humanos atualmente conhecidas. Apesar de a oncogenicidade do poliomavírus ser largamente relatada na literatura desde 1950, a primeira descrição de poliomavírus como agente etiológico de neoplasia em humanos foi feita apenas em 2008, com a descrição do MCPyV, presente em cerca de 80% dos casos de carcinoma de células Merkel (CCM), com a integração de seu genoma ao das células tumorais e mutações tumor‐específicas, sendo considerado o agente etiológico dessa neoplasia desde então. O MCPyV também já foi detectado em carcinomas de queratinócitos, como o carcinoma basocelular e o carcinoma de células escamosas da pele em indivíduos com e sem imunossupressão. Dados sobre a ocorrência de viroses oncogênicas e potencialmente envolvidas na oncogênese, que causam persistência e injúria tecidual, relacionados ao poliomavírus de células de Merkel ainda são escassos, permanecendo em aberto a hipótese de que o poliomavírus de células de Merkel possa ter papel relevante na gênese de outros carcinomas cutâneos além do CCM. Portanto, o artigo se propõe ao aprofundamento no estado atual de conhecimento sobre a presença do MCPyV em carcinomas de queratinócitos.
Estima‐se que em torno de 16% de todos os casos de câncer no mundo estão relacionados a agentes infecciosos, e aproximadamente 10% a 12% desses casos estão associados aos vírus.1–3 Os oncovírus humanos, vírus identificados como agentes etiológicos de alguns tipos de câncer e com capacidade oncogênica inequívoca, amplamente aceitos pela comunidade científica atualmente, são: os papilomavírus humanos (HPV); vírus da hepatite B; vírus da hepatite C; vírus Epstein‐Barr; herpes‐vírus humano 8; vírus linfotrópico de células T humanas (HTLV) e poliomavírus de células de Merkel (MCPyV).4,5 Essa conclusão é feita com base no conhecimento acumulado de um grande número de estudos experimentais, clínicos e epidemiológicos das últimos cinco décadas.1–5 Apesar de muitas viroses animais e humanas poderem transformar células normais em oncogênicas, ainda há poucas viroses consistentemente associadas às neoplasias nos humanos. Dentre os vírus que causam infecção persistente e que têm comprovado potencial oncogênico, destacam‐se os poliomavírus (PyV), que são, com frequência, encontrados em lesões neoplásicas.
É notável, também, que em virtude da onipresença e persistência desses vírus, sua associação causal com essas neoplasias e outras lesões não neoplásicas variadas é de difícil interpretação. Postula‐se que a reativação e cronificação dessas infecções possam estar relacionadas ao processo de malignização em decorrência da injúria tecidual crônica. Além disso, tem sido relatada a presença concomitante desses agentes virais em alguns tumores, indicando possível papel coestimulatório do processo infeccioso.1
A oncogênese é via multifatorial, e sistemas virais suportam a noção de que o desenvolvimento do tumor ocorre pelo acúmulo de eventos múltiplos, enquanto a presença do DNA viral nas células tumorais não é, necessariamente, um fator causal. A transformação celular causada pela infecção viral pode conduzir à ativação de oncogenes ou à inativação de genes supressores de tumor, tornando‐se mecanismos importantes na oncogênese viral.6,7 A produção de proteínas oncogênicas consiste no principal mecanismo oncogênico de alguns retrovírus, enquanto a inativação de proteínas supressoras de tumor ocorre em alguns vírus de DNA como os PyV. Para esses, a inibição e degradação das proteínas regulatórias como a proteína p53 e a proteína do retinoblastoma consiste em sua principal estratégia.6,7 Além disso, a inflamação crônica, muitas vezes causada por outros agentes infecciosos, pode levar ao aumento do risco de câncer, como nos casos de câncer de cólon na colite ulcerativa. A competência do sistema imune também é fundamental para o controle do processo infeccioso e oncogênico; a imunossupressão é um dos principais fatores de risco de progressão para neoplasias.6,7
Desde a descoberta do MCPyV, em 2008,8 considerado o primeiro PyV humano inequivocamente relacionado à uma neoplasia em humanos, o carcinoma de células de Merkel (CCM), uma neoplasia rara, de origem possivelmente neuroendócrina e de curso agressivo, a detecção do seu genoma viral começou a ser investigada não apenas em casos de CCM, mas também em diversas outras neoplasias cutâneas, denominados de câncer de pele não melanoma (CPNM) ou carcinoma de queratinócitos (CQ), como o carcinoma basocelular (CBC) e o carcinoma cutâneo de células escamosas (CEC), o que despertou grande interesse de diversos pesquisadores.9–13
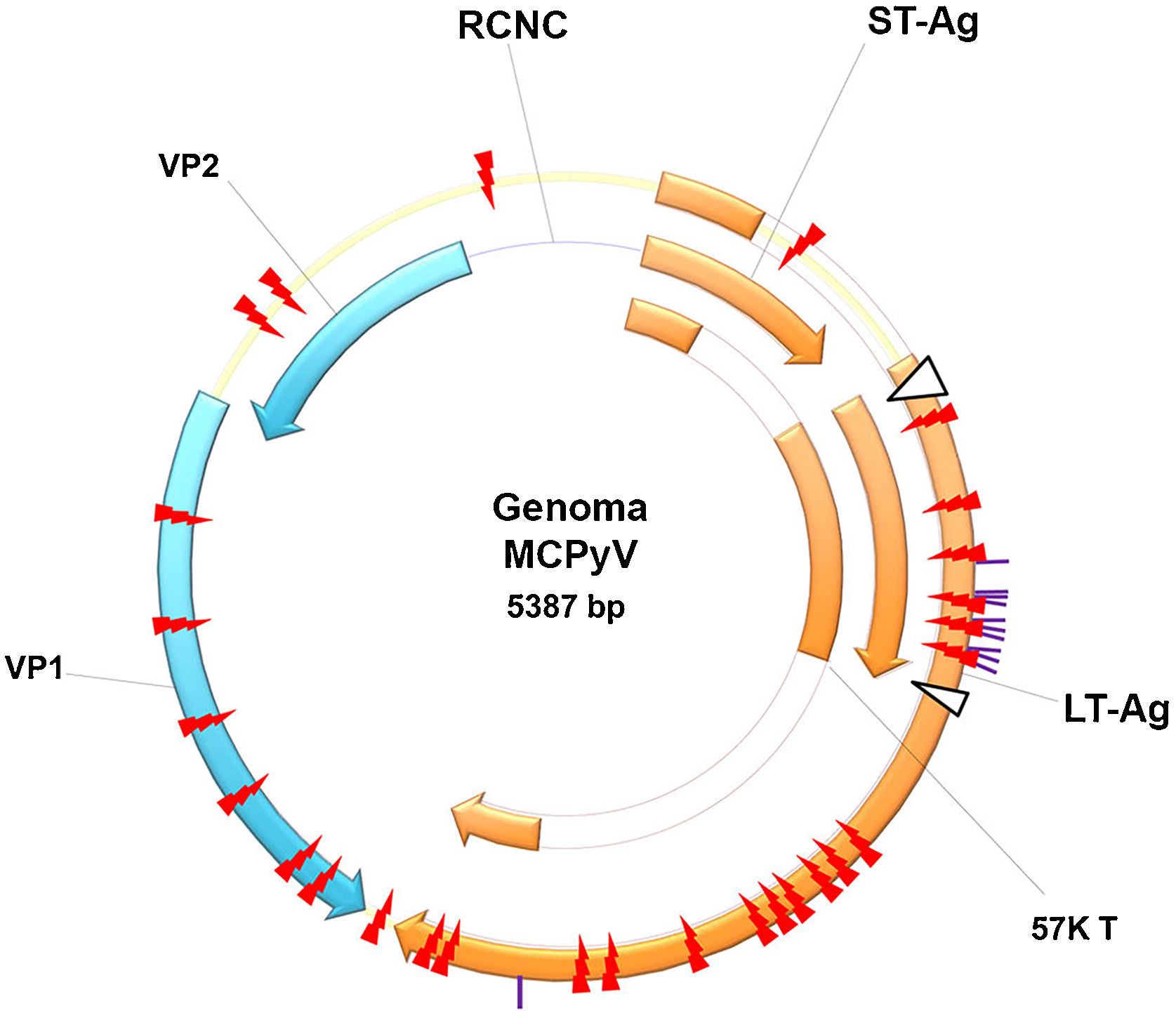
História do poliomavírus e do poliomavírus de células de MerkelO primeiro PyV foi isolado em 1953 por Ludwik Gross, e recebeu esse nome por ser agente causal de múltiplos tumores em roedores (do grego poli: múltiplos; oma; tumores). Desde então, foram descobertas novas espécies de PyV, que infectam mamíferos, pássaros e peixes.14 São vírus não envelopados, icosaédricos, com tamanho aproximado de 45nm, com DNA de dupla fita. Seu genoma viral é dividido em três regiões principais: região controle não codificante (RCNC ou NCCR, non coding control region), responsável pelos elementos para regulação da replicação e transcrição viral; região de codificação inicial (early region), que codifica o antígeno‐T maior (Large T antigen ou LT‐Ag) e o antígeno‐T menor (small T antigen ou sT‐Ag); e região de codificação tardia (late region), que codifica as proteínas estruturais expressas após o início da replicação do DNA: proteína do capsídio viral 1 ou VP1, proteína do capsídio Viral 2 ou VP2 e proteína do capsídio viral 3 ou VP3, que formam o capsídio viral (fig. 1).15
Genoma do MCPyV: região controle não codificante (NCCR, non coding control region); região de codificação inicial (early region), que codifica os antígeno‐T maior (LT‐Ag) e T‐small (sT‐Ag); e região de codificação tardia (late region). LT‐Ag, Large T‐antigen ou antígeno‐T maior; sT‐Ag, small‐T antigen ou antígeno‐T menor; RCNC, região controle não codificante ou non‐coding control region; VP1 e VP2, proteína do capsídio viral 1 e 2. Fonte: reproduzida de Liu W et al., 2016.15
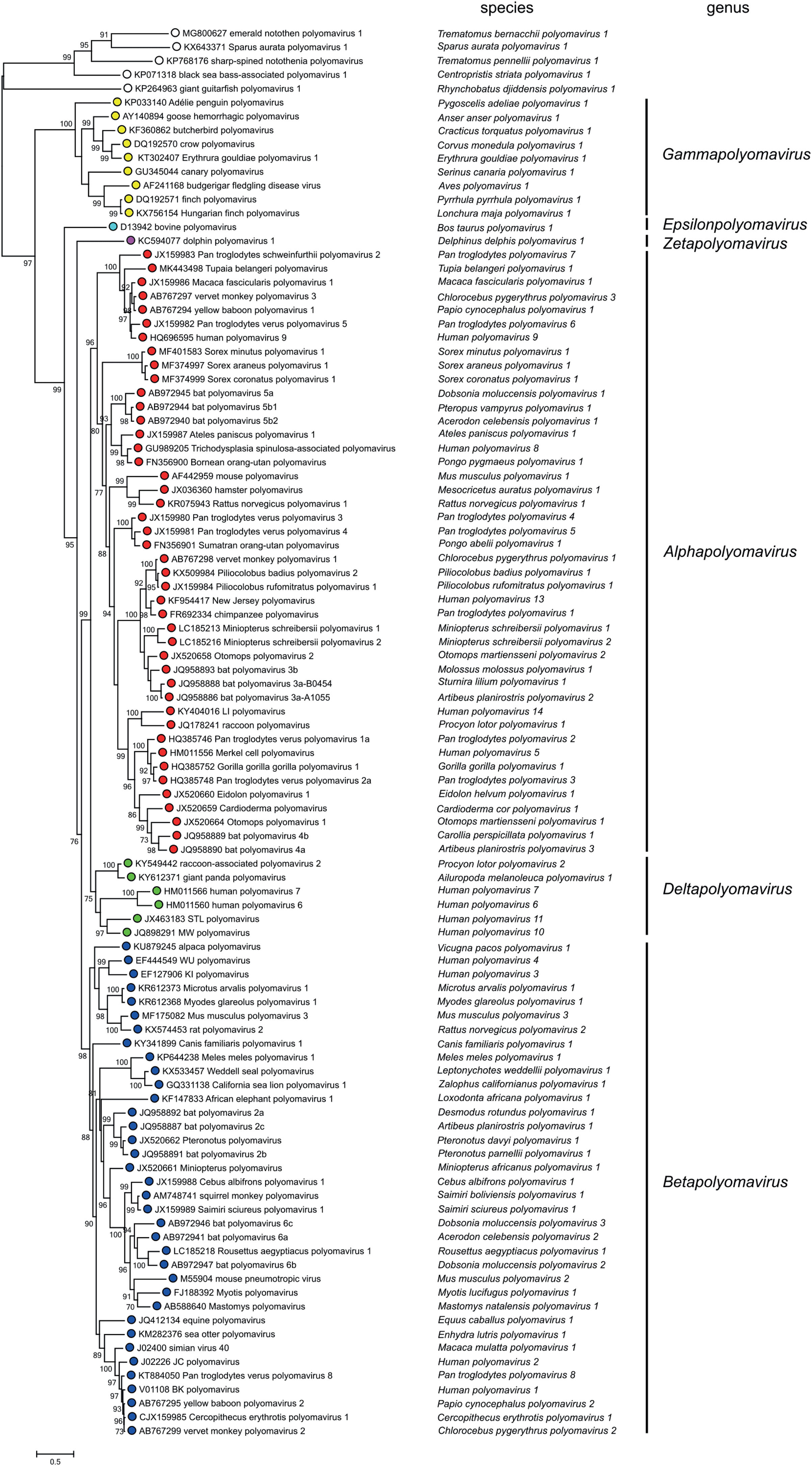
O ritmo em que os PyV estão sendo descobertos aumentou enormemente nos últimos 10 anos, havendo constantes atualizações e revisões na taxonomia realizadas pelo Comitê Internacional de Taxonomia de Vírus (ICTV).14 Atualmente, divide‐se a família Polyomaviridae em seis gêneros e 117 espécies com base nas relações filogenéticas da sequência de aminoácido do LT‐Ag: Alphapolyomavirus, Betapolyomavirus, Gammapolyomavirus, Deltapolyomavirus, Epsilonpolyomavirus e Zetapolyomavirus, acrescido de um grupamento de espécies ainda sem gênero definido.16 O gênero Alphapolyomavirus reúne espécies de PyV que infectam humanos e animais, incluindo os poliomavírus humanos (HPyV) 5 ou MCPyV, HPyV8 ou poliomavírus associado a tricodisplasia spinulosa (TSPyV), HPyV9, HPyV12 e HPyV13; o gênero Betapolyomavirus conta com espécies que infectam humanos e animais, incluindo HPyV1 e HpyV4; o gênero Deltapolyomavirus contém os HPyV6, HPyV7, HPyV10 e HPyV11; o gênero Gammapolyomavirus, Epsilonpolyomavirus e Zetapolyomavirus, descritos recentemente, reúnem outras espécies que infectam mamíferos e peixes, somando‐se ainda as espécies de PyVs sem gênero definido (fig. 2).14,16,17
Revisões na taxonomia dos PyV pelo Comitê Internacional de Taxonomia de Vírus (ICTV), incluindo mais de 100 espécies e dividindo a família Polyomaviridae em seis gêneros, acrescido de um grupamento de espécies sem gênero definido: Alphapolyomavirus, Betapolyomavirus, Gammapolyomavirus, Deltapolyomavirus, Epsilonpolyomavirus e Zetapolyomavirus. Fonte: Moens U et al.16
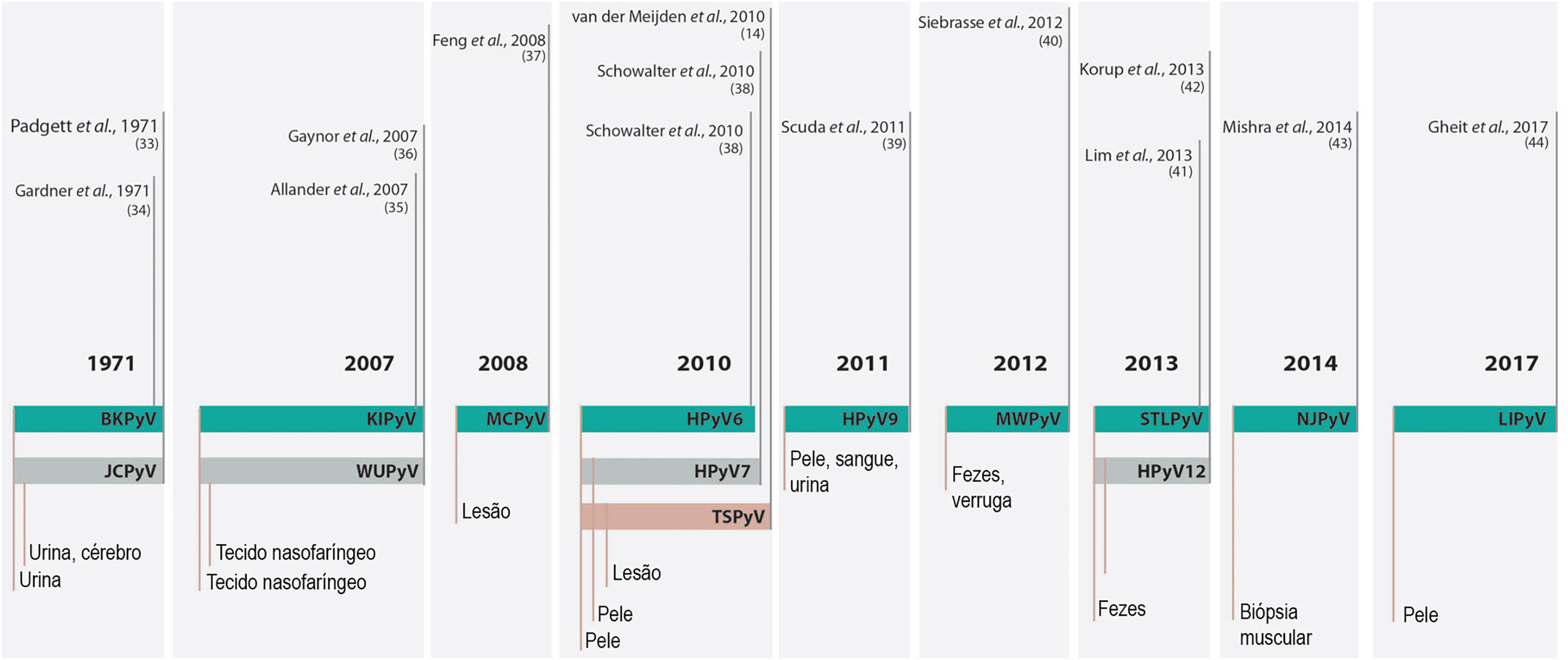
Até 2007, somente duas espécies haviam sido descritas como membros da família que infectavam humanos: o HPyV1 ou poliomavírus BK (BKPyV), e o HPyV2 ou John Cunningham poliomavírus ou Vírus JC (JCPyV). Dessa data em diante, em virtude da evolução da tecnologia para sequenciamento genético, outros 12 HPyV foram descritos e nomeados conforme a ordem cronológica de sua descoberta, totalizando as 14 espécies que infectam humanos conhecidas atualmente (fig. 3).16–18
Cronologia de 14 espécies de PyV que infectam humanos descobertas desde 1971. Fonte adaptada: Prado J et al., 2018.18
Diversas dessas espécies têm afinidade pelo tecido cutâneo, incluindo o HPyV6, HPyV7, HPyV9, TSPyV e o MCPyV.19–22 Sabe‐se que doenças significantes causadas por PyV ocorrem em pacientes imunossuprimidos, como leucoencefalopatia multifocal progressiva em pacientes com síndrome da imunodeficiência adquirida pelo JCPyV, cistite hemorrágica em pacientes após transplante alogênico de células‐tronco hematopoéticas pelo BKPyV, entre outros. Cerca de 10% dos pacientes transplantados renais desenvolvem nefropatia associada ao BKPyV, com perda de função do enxerto em até 50% dos casos da doença.23
Classificação criada pela Agência Internacional de Pesquisa em câncer (International Agency for Research on Cancer – IARC) da Organização Mundial de Saúde (OMS) divide os agentes carcinogênicos em grupos, separados pela sua maior ou menor ação carcinogênica em humanos, baseados em evidência: Grupo 1 como agentes carcinogênicos em humanos; Grupo 2A como agentes provavelmente carcinogênicos em humanos; Grupo 2B como agentes possivelmente carcinogênicos em humanos; Grupo 3 como agentes não relacionados à carcinogênese em humanos. Entre os agentes virais envolvidos ou potencialmente copartícipes na oncogênese, encontram‐se os HPyV, notadamente o MCPyV. Com base nessa classificação da OMS, o MCPyV foi classificado como sendo do Grupo 2A.5,24,25
Evidências sorológicas suportam a persistência da infecção pelos HPyV. Pela medição de anticorpos contra a proteína VP1 do capsídio viral, pode‐se inferir que a exposição ao HPyV ocorre na infância, com aumento da soroprevalência ao passar dos anos, medindo‐se níveis muito baixos até os 18 meses de vida e próximos dos 80% aos 5 anos de idade.8 Ensaios sorológicos realizados especificamente para o MCPyV também confirmam essa onipresença viral, em que 80% dos adultos apresentavam anticorpos contra o vírus.26
A presença do DNA do MCPyV, detectada em cargas virais variáveis pela técnica de PCR, também tem sido descrita em diversos tecidos não tumorais, como na pele, sangue periférico, tratos gastrintestinal, respiratório e urinário, glândula suprarrenal, baço, medula óssea, estômago, vesícula biliar, pâncreas, coração e aorta, embora com índice relativamente baixo de carga viral, entre 0,00026 e 0,22 cópias por célula.27–30 Em média, o número de cópias do genoma viral de MCPyV foi 60 vezes menor em tecidos saudáveis quando comparados com amostras de CCM.28
Outro fator que reforça que a infecção pelo MCPyV seja onipresente e assintomática é o de que 60% a 80% da população eliminem continuamente o MCPyV através da pele saudável.31 Relatos recentes também reportam que os fibroblastos presentes na derme podem suportar a replicação viral e podem ser células hospedeiras genuínas para esse vírus.32
Carcinoma de células de Merkel e poliomavírus de células de MerkelApesar de a oncogenicidade do PyV ser largamente relatada na literatura desde 1950, a primeira descrição de PyV como agente etiológico de neoplasia em humanos foi feita apenas em 2008, com a descrição do MCPyV, presente em cerca de 80% dos casos de CCM e agente etiológico desse tumor.8
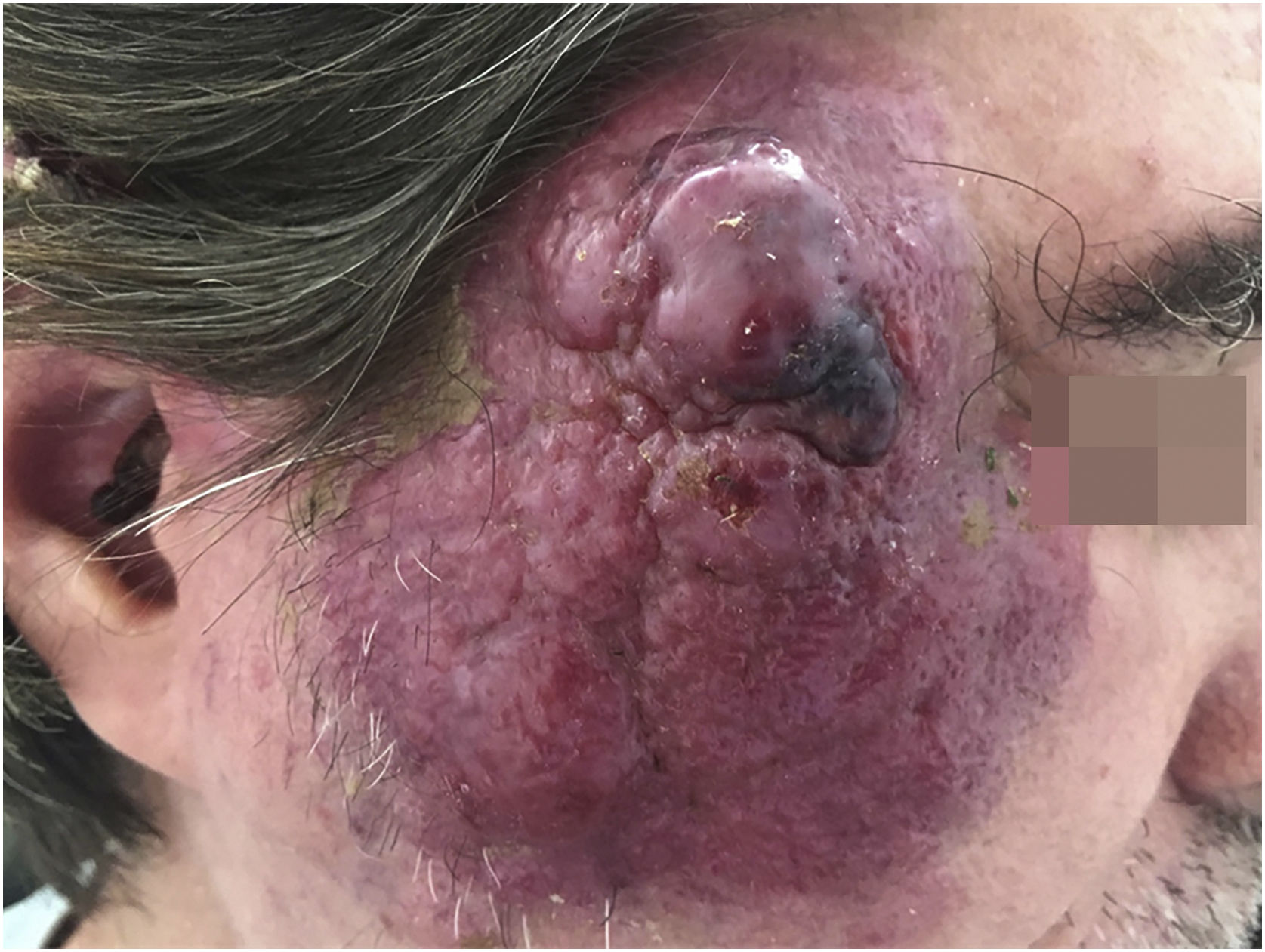
O CCM é neoplasia rara, de origem possivelmente neuroendócrina, com curso agressivo, e normalmente acomete pacientes de idade avançada, imunossuprimidos, em locais de fotoexposição crônica. A lesão costuma se apresentar como pápula ou nódulo eritematoso, de crescimento rápido e sem sintomas associados. A maioria dessas lesões apresenta três ou mais características resumidas no acrônimo AEIOU: A de “Asymptomatic nodule” ou nódulo assintomático; E de “Expanding rapidly” ou expansão rápida; I de “Immunosuppressed host” ou hospedeiro imunossuprimido; O de “Older than age 50” ou idade acima de 50 anos; e U de “UV exposed sitesor fair skin” ou locais fotoexpostos aos raios ultravioletas (UV) ou pele clara33 (fig. 4).
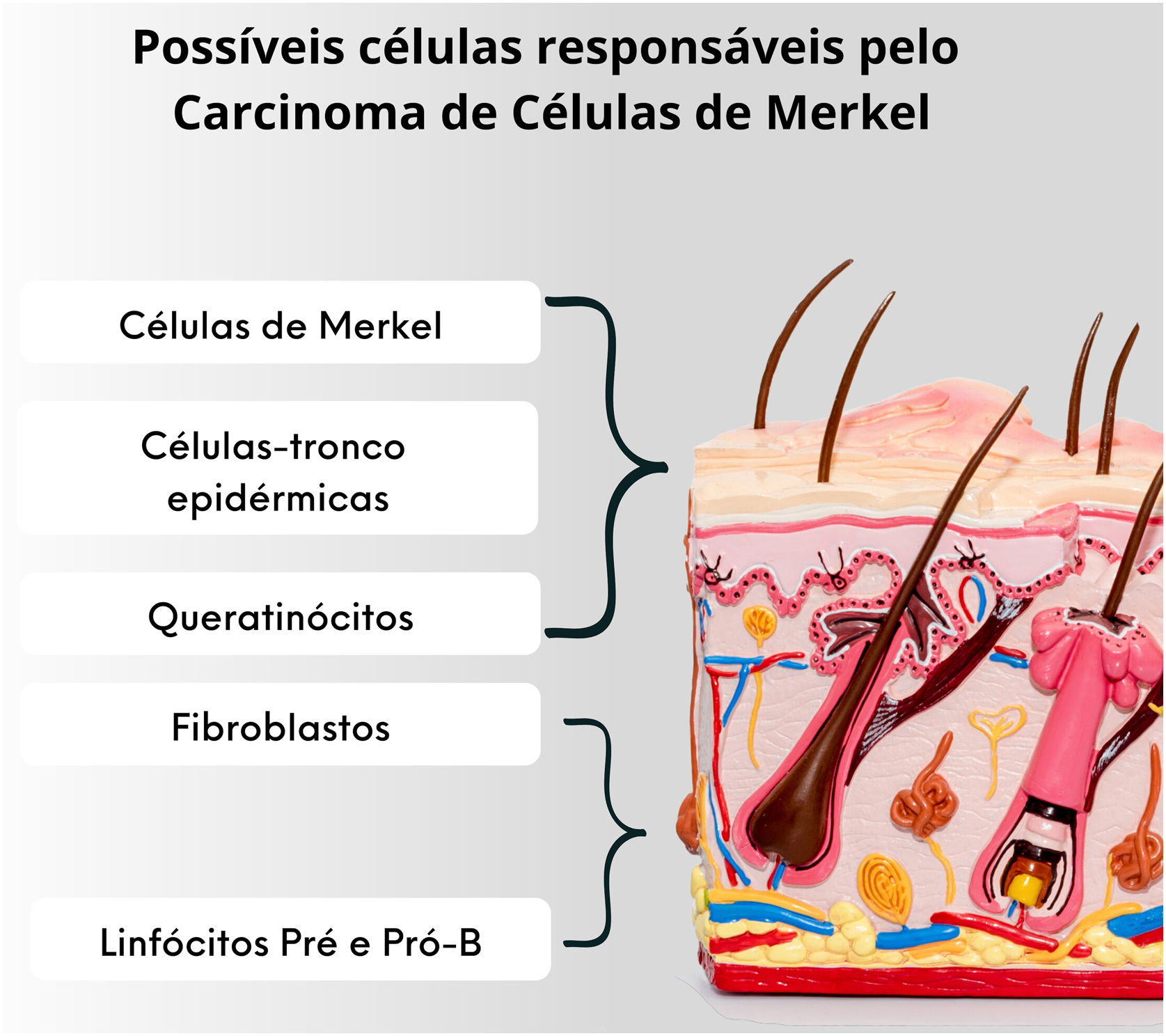
Apesar de as células tumorais compartilharem características morfológicas e histológicas com as células de Merkel, há um debate sobre a origem desse tumor. Isso se deve ao fato de que as células de Merkel são pós‐mitóticas, estando em estágio de diferenciação terminal e não realizando mitoses, o que dificulta bastante a origem de um tumor. Outro questionamento é que o CCM raramente acomete os locais onde há células de Merkel, como palmas, plantas, leito ungueal e mucosa oral e genital. Somam‐se a esse fato a ausência de descrição de lesões displásicas ou precursoras desse tumor, a localização das células de Merkel na epiderme, enquanto o CCM se localiza na derme, a diferença de fenótipos entre a célula de Merkel e o CCM. Desse modo, postula‐se que outras células possam ser responsáveis pela origem desse tumor, e os possíveis candidatos incluem células‐tronco epidérmicas, queratinócitos (as células predominantes em todas as camadas de células epidérmicas), fibroblastos dérmicos, células pró‐B ou células pré‐B (fig. 5).4,33,34
Nessa rara neoplasia cutânea, o DNA viral se integra clonalmente ao DNA da célula hospedeira pelo resultado de mutação. O padrão de integração clonal do DNA do MCPyV ao DNA da célula hospedeira sugere que a infeção viral ocorreu anteriormente à expansão clonal das células neoplásicas do CCM.15 Em adição a essa mutação que causou a integração clonal, uma segunda mutação é necessária para o desenvolvimento dessa neoplasia, o que justifica em parte a raridade dessa entidade. A segunda mutação pode ser induzida pela exposição aos raios UV e é representada pela truncagem do LT‐Ag do MCPyV. Essa mutação, em última análise, levará a uma inibição da proteína supressora de tumor RB nessas células infectadas, acarretando no aumento dos fatores de transcrição E2F e desencadeamento da fase S do ciclo celular, de maneira semelhante ao que ocorre no mecanismo de oncogênese pela oncoproteína E7 do HPV. O LT‐Ag também contribui para a oncogênese por meio do estímulo à angiogênese e à atividade da telomerase, além da inibição de vias intracelulares que levam à apoptose. O sT‐Ag também parece ter múltiplas funções oncogênicas e agiria em conjunto com o LT‐Ag para a conclusão desse processo.35 Feng et al.8 descrevem a integração do genoma do MCPyV ao genoma celular anteriormente à expansão clonal das células neoplásicas, além dessas mutações tumor‐específicas de truncagem do LT‐Ag.8,36 Tais mutações têm sido relatadas também em uma parcela de leucemia linfocítica crônica37 e câncer de pulmão de células não pequenas.38 O genoma viral também foi encontrado em câncer de células escamosas e adenocarcinomas cervicais39 e leucemias linfoides,40,41 embora não exista ainda comprovação etiológica do MCPyV em malignidades diferentes de CCM.
Estudos recentes têm dado maior relevância ao papel oncogênico do sT‐Ag do que se pensava anteriormente. Uma diferença fundamental entre o MCPyV e outros PyV é que o sT‐Ag parece estar diretamente envolvido na transformação neoplásica induzida por MCPyV no CCM.42
Liu et al.,32,42 depois de examinar queratinócitos epidérmicos, fibroblastos dérmicos, células de Merkel e muitos outros tipos de células na pele, descobriram que apenas os fibroblastos dérmicos são permissivos à entrada, transcrição e replicação do MCPyV.32,42 Esses fibroblastos, quando tratados com fator de crescimento epidérmico e fator de crescimento básico de fibroblastos, foram particularmente eficazes no suporte à infecção pelo MCPyV, e como esses fatores de crescimento costumam ser tipicamente regulados positivamente em locais de feridas cutâneas, sugere‐se que o processo de cicatrização possa induzir um microambiente tecidual propício à infecção e replicação do MCPyV.32,42
Tem sido sugerido, em estudos inicialmente realizados na população australiana, que a participação do MCPyV na gênese do CCM seja pouco frequente em tumores localizados em áreas fotodanificadas de indivíduos de pele clara.43 Essa informação é corroborada pela menor frequência de detecção do DNA viral em casos de CCM associados à diferenciação escamosa, que costuma ocorrer apenas em áreas fotodanificadas, levando à hipótese de que haja uma via alternativa de oncogênese nesses tumores independente do vírus.44,45
A taxa de positividade viral vista em tumores de regiões com e sem fotoexposição também foi estudada por Dabner et al.,46 utilizando‐se como parâmetros histológicos a elastose solar na derme e a displasia epidérmica como sinais de dano actínico crônico. Os resultados demonstram o mesmo padrão, com menor presença viral em tumores de áreas fotoexpostas. Em consonância, Paik et al.45 também demonstraram menor positividade do MCPyV em CCM por imuno‐histoquímica em indivíduos australianos, com taxa de detecção de 7,7% (3 em 39) nos tumores localizados na cabeça e pescoço e de 24,6% (16 em 65) em outras localizações do corpo. Esses estudos reforçam a possibilidade de que os tumores localizados em regiões fotoexpostas, como cabeça e pescoço, tenham outras vias de carcinogênese não relacionadas à presença viral, o que explicaria a baixa detecção por esse método nesses tumores.45
No entanto, há estudos que apontam na direção contrária, demonstrando maior presença do DNA viral, por meio da técnica de PCR, em CPNM de locais fotoexpostos. Esse resultado levanta a hipótese de que a carcinogênese viral age como fator complementar à carcinogênse induzida pela radiação UV.47
Até o presente momento, ainda não existe um teste padrão‐ouro para a detecção do MCPyV, e mesmo a utilização combinada de PCR e imuno‐histoquímica (IHQ) tem resultados subótimos.48 Estudos anteriores que utilizaram as duas técnicas combinadas para a detecção do MCPyV em CCM tiveram maior positividade com a técnica de PCR, o que sugere sua maior sensibilidade.44,49–52 No entanto, outros autores descreveram a detecção do MCPyV em CCM com técnicas combinadas em que houve maior detecção viral por meio da IHQ – os autores atribuíram esse achado à grande diversidade de metodologias na técnica de PCR para o MCPyV, como utilização de primer com diferentes sequências genéticas, número de conjuntos de primers do vírus detectado, diferenças na sequência humana de referência que é amplificada e os limites de corte usados para considerar um teste positivo. É possível que o ensaio de PCR mais sensível e específico para detecção de MCPyV ainda não tenha sido comparado com os ensaios de IHC.48
Câncer de pele não melanoma e carcinoma de queratinócitos relacionados ao poliomavírus de células de MerkelO câncer de pele não melanoma (CPNM) ou CQ engloba basicamente todas as malignidades cutâneas que não se referem ao melanoma. No entanto, grande parte desses tumores correspondem ao carcinoma basocelular (CBC), ao carcinoma cutâneo de células escamosas ou carcinoma espinocelular (CEC) e suas variantes.53 O CQ não inclui outros tipos de malignidades cutâneas mais raras e com comportamentos distintos, como o próprio CCM, o dermatofibrossarcoma, linfomas cutâneos, carcinomas sebáceos, angiossarcomas e outros tumores dos anexos cutâneos.54
Considerando o papel do MCPyV no desenvolvimento do CCM e sua detecção em diversos outros tecidos e tumores do corpo humano, alguns pesquisadores começaram a investigar um possível papel etiológico desse vírus na gênese de outros tumores, majoritariamente em CQ.55 Na maioria desses estudos,9–13 o DNA do MCPyV foi detectado pela técnica de PCR, havendo, no entanto, alguns estudos em que o LT‐Ag também foi investigado pela técnica de IHQ, demonstrando na maioria das vezes uma positividade menor do que na técnica de PCR.55
Kassem et al.10 demonstraram a presença do MCPyV pela técnica de PCR em 36 de 96 (37,5%) CBC acometendo pacientes imunocompetentes. Em relação aos CBC de pacientes imunossuprimidos, os valores foram surpreendentemente altos, positivos em 72,2% dos casos. Os mesmos autores descrevem a presença de MCPyV em 7 de 28 casos (25%) de CEC em pacientes imunocompetentes. Semelhante ao que ocorreu com os CBC, o percentual subiu para 52% em pacientes imunossuprimidos. Também foi descrita alta positividade na doença de Bowen (DB), com 17,4% de positividade entre pacientes imunocompetentes e 69% entre pacientes imunossuprimidos.
Ainda em 2009, Dworkin et al.9 descreveram positividade do MCPyV em 26 de 177 (15%) CEC oriundos de pacientes imunocompetentes.9 Além da positividade nos CEC, também se descreveu positividade de 17% na pele adjacente ao tumor (11 de 63 amostras). Houve, entre os casos pareados (tumor e pele adjacente ao tumor), uma concordância (presença ou ausência do DNA viral em ambos os espécimes) de 87%. Esse achado sugere que, apesar da ausência de alterações histológicas específicas, o vírus já poderia estar presente na área perilesional, levando ao futuro desenvolvimento da lesão tumoral.
Zur Hausen et al.56 examinaram um total de 56 CQ oriundos de 11 pacientes imunossuprimidos (25 CEC, 13 DB e 18 CBC) e 147 tumores oriundos de 125 pacientes imunocompetentes (28 CEC, 23 doenças de Bowen e 96 CBC).56 Houve detecção significantemente mais frequente de positividade para MCPyV nos tumores cutâneos de pacientes imunossuprimidos nos três tipos de tumor, com significância estatística (p <0,001). Todos os produtos de PCR também foram sequenciados nesse estudo; as mutações específicas do tumor na área do LT‐Ag não puderam ser detectadas. A carga viral também foi analisada, e na grande maioria dos CQ, a carga viral do MCPyV estava bem abaixo dos casos de CCM positivos para MCPyV usados como controles.56
Wieland et al.57 analisaram a presença do MCPyV pela técnica de PCR em 355 amostras de pele, incluindo uma grande gama de CQ, melanomas, lesões benignas e pele sadia perilesional.57 Houve positividade para a presença viral em três dos 21 CBC (14%), um de seis CEC (17%), um de quatro doenças de Bowen (25%), três de sete ceratoacantomas (43%), dois de 12 melanomas (17%), nenhum caso positivo em verrugas virais e ceratoses actínicas, e oito de 34 casos de detecção em pele sadia perilesional (24%). O DNA viral foi encontrado em 30 dos 34 casos de CCM utilizados como controle, e com carga viral maior do que a encontrada nos CQ, resultado similar ao descrito por Zur Hausen et al.56,57
Garneski et al.43 encontraram uma taxa de 13% de positividade do MCPyV em CEC, em que duas das 15 lesões de CEC estudadas albergavam o DNA viral.43 Em contrapartida, Reisinger et al.58 pesquisaram a positividade do LT‐Ag por IHQ, utilizando o anticorpo CM2B4 em 20 pacientes com CCM e em alguns CBC e CEC oriundos desses mesmos pacientes. Um total de 12 desses pacientes apresentavam CBC e CEC que se desenvolveram após a detecção do CCM; a pesquisa do LT‐Ag por IHQ utilizando o anticorpo monoclonal CM2B4 veio negativa em todos os 12 casos. De maneira oposta, esses pacientes tinham alta positividade de 92% (11 em 12) para o LT‐Ag visto por IHQ em seus CCM.58 Rollison et al.59 descreveram um percentual de 38% de positividade do MCPyV DNA em amostras de tecido congelado fresco de CEC obtidos de pacientes imunocompetentes. A presença do MCPyV DNA se associou a altos níveis de anticorpos anti‐MCPyV circulantes.59 Esse expressivo percentual em pacientes imunocompetentes pode ser decorrente do fato de as amostras terem sido estudadas imediatamente após sua retirada e não após processamento do material em blocos de parafina, evitando a possível degradação parcial do material genético presente.
Em consonância com esses estudos, Mertz et al.60 detectaram o DNA do MCPyV por PCR em dois (10%) de 20 pacientes com DB. Em um desses pacientes, que era imunossuprimido por transplante renal, foram também avaliadas diversas outras lesões cutâneas, com positividade para o MCPyV em quatro de quatro verrugas virais (100%), três de seis doenças de Bowen (50%), e duas de três ceratoses seborreicas (66,6%). Em uma segunda coorte realizada em pacientes imunossuprimidos e submetidos a transplante renal, o DNA do MCPyV foi encontrado em uma de 16 verrugas virais (6,3%), em duas de 21 Doenças de Bowen (9,5%). Em indivíduos imunocompetentes, o DNA do MCPyV foi encontrado em duas das 30 verrugas virais (6,7%) e em duas das 24 Doenças de Bowen (8,3%).60
Os mesmos pesquisadores,13 em 2013, encontraram positividade para o vírus em 28 de 71 (39,4%) CBC retirados de pacientes imunocompetentes. Essa taxa subiu para 47,1% em imunossuprimidos, em que oito de 17 CBC albergavam o DNA viral. Em contraste com a frequente detecção viral por PCR nese estudo, a IHQ para a pesquisa do LT‐Ag no tecido tumoral foi positiva apenas em dois dos 17 casos de CBC que acometiam pacientes imunossuprimidos, e negativa em todos CBC dos pacientes imunocompetentes.13 Nesse mesmo ano, Murakami et al.61 encontraram quatro de 30 (13%) CEC positivos para MCPyV; desses quatro, dois também eram positivos para LT‐Ag pela IHQ. Também foi descrito no mesmo estudo uma total negatividade para a presença do MCPyV pela PCR em 10 casos de CBC, não obstante o fato do pequeno número total de casos dificultar a análise.
Becker et al., após confirmarem a presença do MCPyV em 45 de 53 (84,9%) pacientes com CCM, descreveram positividade viral em três de 24 (12,5%) casos de CBC.62
Neto et al.62 também fizeram análise recente entre a presença de MCPyV e tumores cutâneos, analisando 10 casos de CBC e 10 de CEC. Pela técnica de PCR com extração do material genético de material guardado em bloco de parafina, foi detectado material genético do MCPyV em quatro dos 20 casos, em comparação com a presença em 100% dos 20 casos de CCM analisados também nesse estudo.63
Ridd et al.,63 após investigarem a presença do DNA do MCPyV por PCR em 85 casos de CEC, 37 ceratoacantomas, 28 doenças de Bowen e seis ceratoses actínicas, encontraram positividade apenas em um caso de ceratoacantoma. A técnica de PCR desse estudo foi validada em uma coorte de CCM, que demonstrou 54% (7/13) dos tumores positivos para a presença do MCPyV.64
Kaibuchi‐Noda et al.65 descreveram um relato de caso em que um paciente imunossuprimido, um ano após ter CEC ressecado, apresentou metástases diagnosticadas como CCM, tendo realizado a pesquisa do DNA do MCPyV por PCR e do LT‐Ag por IHQ.65 O estudo revelou que o DNA do MCPyV foi detectado na lesão de CEC, indicando que a infecção pelo MCPyV ocorrera pelo menos um ano antes da ocorrência de CCM metastático. No entanto, o número de cópias do MCPyV por célula na lesão de CCM foi maior que na de CEC, e a pesquisa do LT‐Ag pela IHQ foi positiva apenas no CCM, colocando em dúvida se houve participação efetiva do MCPyV na gênese de ambos os tumores ou se apenas no CCM.65
Estudos recentes também indicam a presença de outros HPyV em ceratoacantomas e outros CQ. Beckervordersandforth et al.66 descreveram a presença do HPyV6 por PCR em diversos tumores incluídos no grupo de CPNM; 25 dos 59 (42,3%) dos ceratoacantomas apresentavam material genético, assim como 23 dos 109 (21,1%) casos de CBC e oito dos 86 (9,3%) casos de CCE.66
A presença do HPyV6, assim como a de outros HPyV, como o MCPyV, TSPyV, HPyV6, HPyV7, HPyV9 e HPyV10, também foi investigada em CEC de pacientes com melanoma em tratamento com inibidores de BRAF.67 Até o momento, os únicos fatores identificados que contribuem para o desenvolvimento de CEC nesses pacientes são mutações nos genes RAS. No entanto, essas mutações explicam apenas 60% dos tumores. É importante identificar o que está causando os tumores remanescentes. Dezoito amostras de biopsia de seis pacientes foram avaliadas, 10 (62%) das 16 amostras continham mutações RAS; o DNA de HPyV9, HPyV10 e TSPyV estava ausente nas amostras, o DNA do MCPyV estava presente em 13 das 18 amostras (72,22%); e o DNA do HPV, HPyV6 e HPyV7 estava presente em todas as amostras. Em geral, a carga viral encontrada nesse estudo foi baixa, com exceção do HPyV6, que também foi detectado por IHQ com os antígenos da proteína central VP1.67 Haeggblom et al. descreveram a presença de PyV em ceratoacantomas e nevos de Spitz e, apesar de não haver predominância de nenhuma espécie específica, foi encontrado material genético viral pela técnica de PCR em 20 de 47 lesões dessas afecções.68
Estudo realizado por Toptan et al.69 investigou, por meio de um anticorpo utilizado na técnica de IHQ que detecta simultaneamente uma ampla gama de HPyV, incluindo o MCPyV, a presença desse vírus em centenas de tumores, dentre eles o CBC e o CEC. Não foi detectada presença do MCPyV nesses carcinomas cutâneos, e raras células marcadas com esse anticorpo em alguns tumores esporádicos foi interpretado como infecção passageira e incidental.69
Estudando 96 lesões cutâneas, Bellott et al.12 detectaram a presença do MCPyV em 31% desses casos, dos quais 23 (33,3%) dentre os 69 casos de CBC, dois dos 11 CEC (18%), duas das quatro doenças de Bowen (50%) e, dentre as outras 11 lesões cutâneas, quatro (36,3%) foram positivos para o DNA viral (duas ceratoses actínicas, um dermatofibrosarcoma e um ceratoacantoma).12 Estudo mais recente pelo mesmo autor,70 dessa vez analisando a presença do genoma viral do MCPyV pela técnica de PCR e do LT‐Ag maior pela técnica de IHQ, teve 103 amostras de CQ de 91 pacientes analisadas. Quarenta e quatro (42,7%) tumores foram positivos para o vírus via PCR, 34 de 85 (40%) no grupo CBC, seis de 12 (50%) no CEC, dois de quatro (50%) para DB e um de dois (50%) para ceratoacantoma. O resultado da IHQ mostra positividade total em 18 casos (17,7%), sete casos de positividade apenas no tumor (6,9%), oito no infiltrado peritumoral (7,9%) e três em ambos (3%).70
Costa et al.71 também realizaram a pesquisa de diversos HPyV por meio da técnica de PCR em tecidos cutâneos, incluindo casos de CQ, melanoma, sarcoma de Kaposi, CCM e pele normal. O MCPyV foi o HPyV mais encontrado, presente em dois de 20 (10%) CBC e três de 20 (15%) CEC, além de não estar presente em um total de 20 casos de pele normal.71
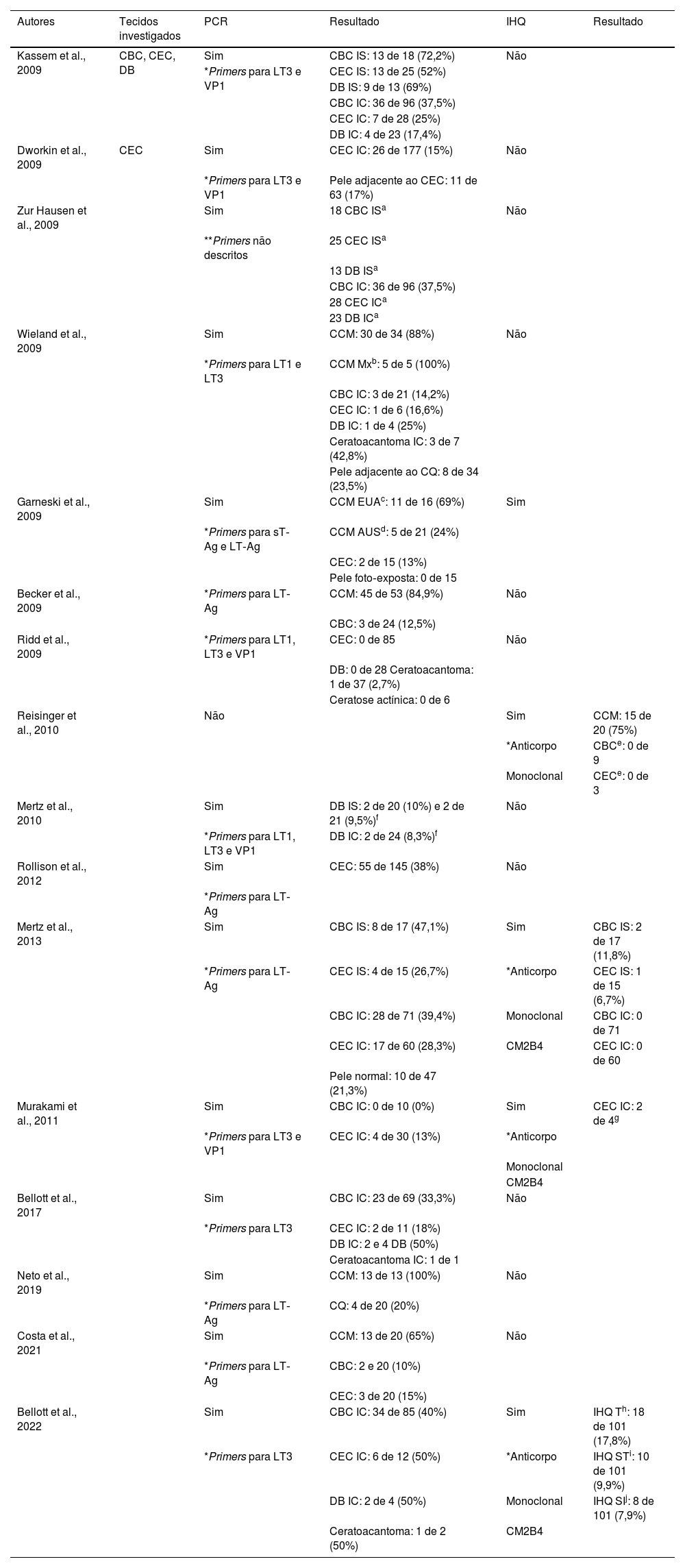
Os principais estudos que investigaram a presença de partículas virais do MCPyV em CQ se encontram reunidos em ordem cronológica na tabela 1.
Principais estudos, em ordem cronológica, que investigam a presença de partículas virais do MCPyV em carcinoma de queratinócitos
| Autores | Tecidos investigados | PCR | Resultado | IHQ | Resultado |
|---|---|---|---|---|---|
| Kassem et al., 2009 | CBC, CEC, DB | Sim | CBC IS: 13 de 18 (72,2%) | Não | |
| *Primers para LT3 e VP1 | CEC IS: 13 de 25 (52%) | ||||
| DB IS: 9 de 13 (69%) | |||||
| CBC IC: 36 de 96 (37,5%) | |||||
| CEC IC: 7 de 28 (25%) | |||||
| DB IC: 4 de 23 (17,4%) | |||||
| Dworkin et al., 2009 | CEC | Sim | CEC IC: 26 de 177 (15%) | Não | |
| *Primers para LT3 e VP1 | Pele adjacente ao CEC: 11 de 63 (17%) | ||||
| Zur Hausen et al., 2009 | Sim | 18 CBC ISa | Não | ||
| **Primers não descritos | 25 CEC ISa | ||||
| 13 DB ISa | |||||
| CBC IC: 36 de 96 (37,5%) | |||||
| 28 CEC ICa | |||||
| 23 DB ICa | |||||
| Wieland et al., 2009 | Sim | CCM: 30 de 34 (88%) | Não | ||
| *Primers para LT1 e LT3 | CCM Mxb: 5 de 5 (100%) | ||||
| CBC IC: 3 de 21 (14,2%) | |||||
| CEC IC: 1 de 6 (16,6%) | |||||
| DB IC: 1 de 4 (25%) | |||||
| Ceratoacantoma IC: 3 de 7 (42,8%) | |||||
| Pele adjacente ao CQ: 8 de 34 (23,5%) | |||||
| Garneski et al., 2009 | Sim | CCM EUAc: 11 de 16 (69%) | Sim | ||
| *Primers para sT‐Ag e LT‐Ag | CCM AUSd: 5 de 21 (24%) | ||||
| CEC: 2 de 15 (13%) | |||||
| Pele foto‐exposta: 0 de 15 | |||||
| Becker et al., 2009 | *Primers para LT‐Ag | CCM: 45 de 53 (84,9%) | Não | ||
| CBC: 3 de 24 (12,5%) | |||||
| Ridd et al., 2009 | *Primers para LT1, LT3 e VP1 | CEC: 0 de 85 | Não | ||
| DB: 0 de 28 Ceratoacantoma: 1 de 37 (2,7%) | |||||
| Ceratose actínica: 0 de 6 | |||||
| Reisinger et al., 2010 | Não | Sim | CCM: 15 de 20 (75%) | ||
| *Anticorpo | CBCe: 0 de 9 | ||||
| Monoclonal | CECe: 0 de 3 | ||||
| Mertz et al., 2010 | Sim | DB IS: 2 de 20 (10%) e 2 de 21 (9,5%)f | Não | ||
| *Primers para LT1, LT3 e VP1 | DB IC: 2 de 24 (8,3%)f | ||||
| Rollison et al., 2012 | Sim | CEC: 55 de 145 (38%) | Não | ||
| *Primers para LT‐Ag | |||||
| Mertz et al., 2013 | Sim | CBC IS: 8 de 17 (47,1%) | Sim | CBC IS: 2 de 17 (11,8%) | |
| *Primers para LT‐Ag | CEC IS: 4 de 15 (26,7%) | *Anticorpo | CEC IS: 1 de 15 (6,7%) | ||
| CBC IC: 28 de 71 (39,4%) | Monoclonal | CBC IC: 0 de 71 | |||
| CEC IC: 17 de 60 (28,3%) | CM2B4 | CEC IC: 0 de 60 | |||
| Pele normal: 10 de 47 (21,3%) | |||||
| Murakami et al., 2011 | Sim | CBC IC: 0 de 10 (0%) | Sim | CEC IC: 2 de 4g | |
| *Primers para LT3 e VP1 | CEC IC: 4 de 30 (13%) | *Anticorpo | |||
| Monoclonal | |||||
| CM2B4 | |||||
| Bellott et al., 2017 | Sim | CBC IC: 23 de 69 (33,3%) | Não | ||
| *Primers para LT3 | CEC IC: 2 de 11 (18%) | ||||
| DB IC: 2 e 4 DB (50%) | |||||
| Ceratoacantoma IC: 1 de 1 | |||||
| Neto et al., 2019 | Sim | CCM: 13 de 13 (100%) | Não | ||
| *Primers para LT‐Ag | CQ: 4 de 20 (20%) | ||||
| Costa et al., 2021 | Sim | CCM: 13 de 20 (65%) | Não | ||
| *Primers para LT‐Ag | CBC: 2 e 20 (10%) | ||||
| CEC: 3 de 20 (15%) | |||||
| Bellott et al., 2022 | Sim | CBC IC: 34 de 85 (40%) | Sim | IHQ Th: 18 de 101 (17,8%) | |
| *Primers para LT3 | CEC IC: 6 de 12 (50%) | *Anticorpo | IHQ STi: 10 de 101 (9,9%) | ||
| DB IC: 2 de 4 (50%) | Monoclonal | IHQ SIj: 8 de 101 (7,9%) | |||
| Ceratoacantoma: 1 de 2 (50%) | CM2B4 |
IS, imunossuprimido; IC, imunocompetente;
CBC e CEC oriundos de pacientes com CCM com IHQ positiva para MCPyV; f Duas coortes realizadas no mesmo estudo; g IHQ realizada apenas nos casos positivos na PCR; h IHQ‐T: marcação total, marcando células do tumor, células do infiltrado linfocítico peri‐tumoral, e ambos; i IHQ‐ST: marcando apenas células do tumor, em associação ou não com células do infiltrado linfocítico peri‐tumoral; j IHQ‐SI: marcando apenas células do infiltrado linfocítico peri‐tumoral.
*Quando os primers foram descritos.
**Quando os primers não foram descritos.
Existem muitas suposições para a variação da prevalência do MCPyV nos CQ entre diferentes estudos e as divergências desses resultados com os de IHQ.
A detecção do DNA do MCPyV pela técnica de PCR pode ser afetada pelos primers que foram usados. De fato, a maioria dos estudos aplicou os primers LT‐Ag originalmente usados por Feng et al.,8 considerados superiores aos primers direcionados contra a VP1.55
A qualidade das amostras também pode afetar o resultado da reação de PCR, pois vários estudos relataram que a detecção do DNA do MCPyV em tecidos frescos congelados é mais confiável quando em comparação com a detecção em amostras fixadas na parafina.55
O DNA viral é extraído de um fragmento do tumor, tendo acesso a somente um subgrupo das células presentes na neoplasia. Há a possibilidade de que haja partículas virais presentes em locais do tumor que não tenham sido analisados em conjunto pela PCR e pela IHQ. O tumor é composto por diversas linhagens celulares heterogêneas que contêm células tumorais, infiltrados celulares imunes como de linfócitos, células endoteliais e fibroblastos associados ao câncer. Sabendo que os fibroblastos podem suportar a replicação viral e podem ser células hospedeiras genuínas para esse vírus,32 e também que os monócitos infiltrados podem ser reservatórios para o vírus,72 produtos de PCR positivos podem derivar de infecção viral nessas células.
Métodos baseados em PCR também são propensos à contaminação, já que se postula que o MCPyV seja eliminado cronicamente pela pele, podendo fazer parte de sua microbiota;73 a contaminação durante a coleta no manuseio das amostras não pode ser excluída.
A detecção simultânea do LT‐Ag pela IHQ e do seu material genético por PCR nesses tecidos tumorais pode demonstrar evidências de uma participação ativa do vírus na manutenção do crescimento cancerígeno, e todos esses estudos demonstram que, para ajudar a elucidar se o MCPyV está realmente associado à gênese dos CQ, mais estudos epidemiológicos ainda são necessários.73
Outras etapas que são ainda importantes para a elucidação dessa questão entre o possível papel etiológico do MCPyV em tumores outros que não o CCM, são:
O estado do genoma do vírus deve ser determinado, se episomal ou integrado, já que a integração do genoma viral parece ser um pré‐requisito para o desenvolvimento do processo neoplásico associado a esse vírus;55
O gene que codifica o LT‐Ag deve ser sequenciado para determinar se há a expressão das mutações tumor‐específicas de do LT‐Ag truncado;55
Hibridização in situ para o DNA ou RNA viral deve ser feita para garantir que as sequências virais sejam detectadas em células tumorais e não em outros tipos de células adjacentes ao tumor.55
Amostras de tumor em diferentes estádios de desenvolvimento também devem ser examinadas, já que o vírus pode estar envolvido apenas no início do processo neoplásico, não sendo necessário para a progressão do tumor.55 De fato, um mecanismo de ataque e fuga para a ação oncogênica do MCPyV em alguns casos de CCM foi sugerido por Houben et al.,74 no qual a oncogênese viral só seria essencial para desencadear o início do processo.74
ConclusãoDiversas informações, como a alta soroprevalência de MCPyV na população humana, os potenciais oncogênicos in vitro do LT‐Ag e do sT‐Ag e seu papel etiológico no CCM, sugerem que o MCPyV pode desempenhar um papel, de maneira isolada ou em associação com outros fatores, em outros tipos de câncer no homem, especialmente em indivíduos com sistema imunológico comprometido; entretanto, essa relação causal entre o MCPyV e CQ ainda não pode ser estabelecida.55
Suporte financeiroO presente estudo faz parte da tese de doutorado do autor principal e foi contemplado com bolsa de pesquisa do FUNADERM (Fundo de Apoio à Dermatologia), órgão da Sociedade Brasileira de Dermatologia.
Contribuição dos autoresThiago Rubim Bellott: Concepção e o desenho do estudo; levantamento dos dados, ou análise e interpretação dos dados; redação do artigo ou revisão crítica do conteúdo intelectual importante; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação final da versão final do manuscrito.
Flávio Barbosa Luz: Concepção e o desenho do estudo; redação do artigo ou revisão crítica do conteúdo intelectual importante; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; aprovação final da versão final do manuscrito.
Anna Karolinne Fausto: Participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; aprovação final da versão final do manuscrito.
Rafael Brandão Varella: Participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; aprovação final da versão final do manuscrito.
Mayra Carrijo Rochael; Participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; aprovação final da versão final do manuscrito.
Luciana Pantaleão: Participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; aprovação final da versão final do manuscrito.
Conflito de interessesNenhum.
Gostaria de agradecer a todos os participantes dessa linha de pesquisa que faço parte no programa de Doutorado, em especial aos orientadores: Flávio Barbosa Luz, Mayra Carrijo Rochael, Luciana Pantaleão, Rafael Brandão Varella e Anna Karolinne Fausto da Silva.
Como citar este artigo: Bellott TR, Luz FB, Silva AKF, Varella RB, Rochael MC, Pantaleão L. Merkel cell polyomavirus and its etiological relationship with skin tumors. An Bras Dermatol. 2023;98:737–49.
Trabalho realizado no Departamento de Patologia, Hospital Universitário Antônio Pedro, Universidade Federal Fluminense, Niterói, RJ, Brasil.