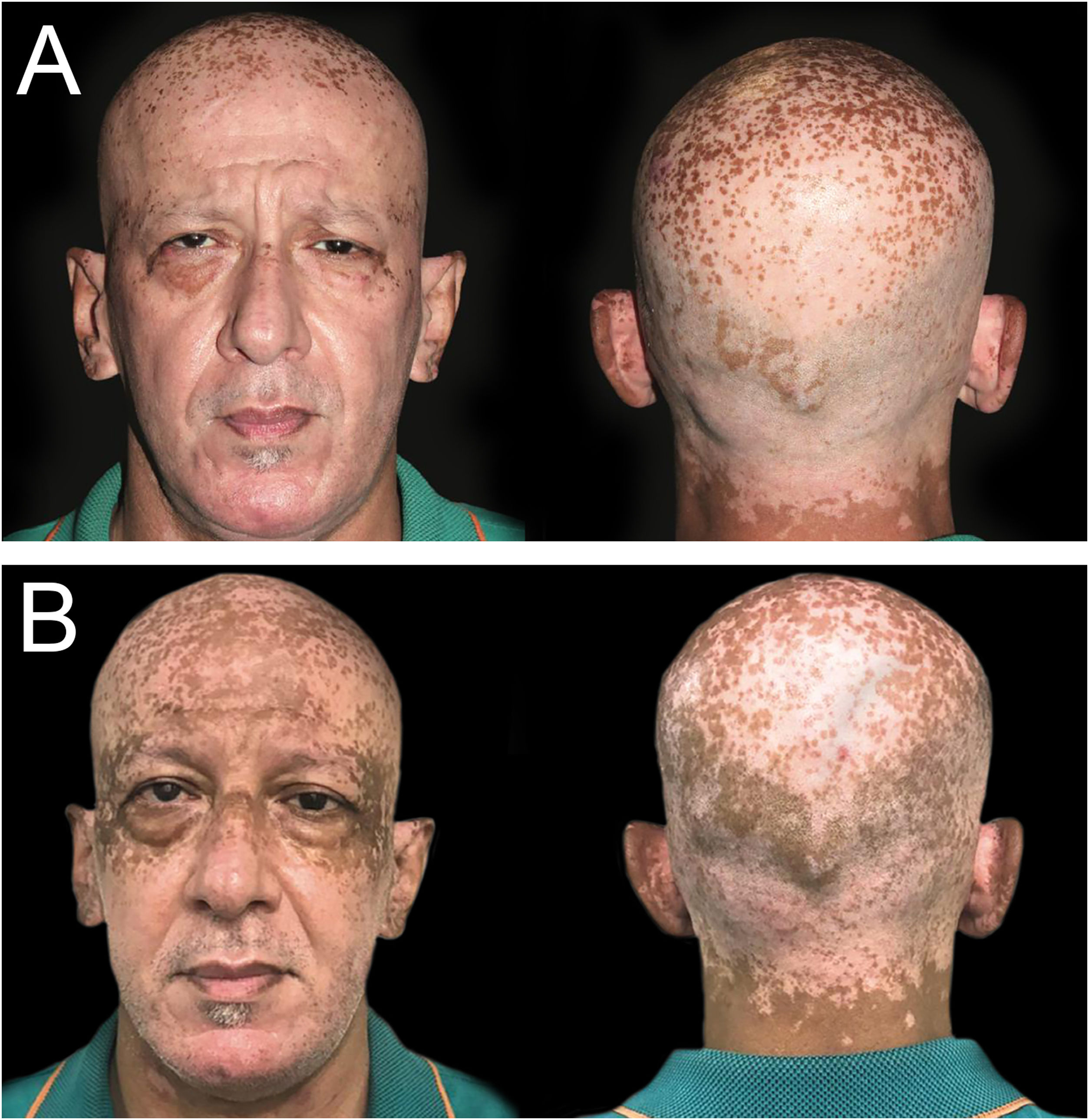
Paciente masculino, de 50 anos, foi atendido no ambulatório de Endocrinologia do Hospital das Clínicas (Universidade de São Paulo) em decorrência de hipertireoidismo em novembro de 2020, encaminhado pela equipe de Cardiologia, que havia iniciado metimazol 15mg/dia dois meses antes. O paciente apresentava história de seis anos de vitiligo generalizado, sem tratamento há três anos. O exame físico revelou tireoide aumentada à palpação, sem nódulos e sem sinais de hipertireoidismo. A pele apresentava máculas e manchas despigmentadas afetando o couro cabeludo, face, região cervical, antebraços, dorso das mãos, dedos, pés e tronco, com alguma hiperpigmentação nas máculas de vitiligo periorbitais e no couro cabeludo (fig. 1A). Com base nos testes de função tireoidiana e ultrassonografia da tireoide (glândula moderadamente hipoecoica sem nódulos, volume de 26,33cm3 e vascularização aumentada), foi estabelecido o diagnóstico de doença de Graves.
(A) Hiperpigmentação de máculas de vitiligo na área periorbital e couro cabeludo, que começou dois meses após o início do metimazol (novembro de 2020). (B) Cinco meses após o início do metimazol, múltiplas máculas e manchas marrons bem demarcadas e dispersas foram observadas em áreas expostas ao sol nos pavilhões auriculares, região frontal, regiões periorbitais e couro cabeludo (fevereiro de 2021).
Os exames laboratoriais antes do metimazol mostraram tireotropina (TSH) <0,008μIU/mL, T4 livre sérico (FT4) 4,99 ng/mL, tri‐iodotironina total (T3) 438 ng/mL, anticorpo do receptor de tireotropina (TRAb) alto (3,88 IU/L) e anticorpo da tireoglobulina indetectável.
Em fevereiro de 2021, enquanto usava metimazol, o paciente mostrou‐se preocupado com a pigmentação recente, surgida dois meses após o início do medicamento. Ele negou vermelhidão, queimação, prurido ou outros sintomas associados. No exame físico, apresentou múltiplas máculas marrons dispersas, bem demarcadas, e manchas em áreas expostas ao sol (pavilhões auriculares, couro cabeludo, região frontal, região periorbital), mais escuras do que a pele normal ao redor, poupando áreas cobertas por máscara facial, utilizada para proteção contra infecção por SARS‐CoV‐2 (fig. 1B). A maioria das outras lesões de vitiligo apresentava alguma repigmentação perifolicular. Os exames laboratoriais mostraram TSH <0,02μIU/mL, FT4 1,85 ng/mL, T3 169 ng/mL e TRAb 2,27 IU/L.
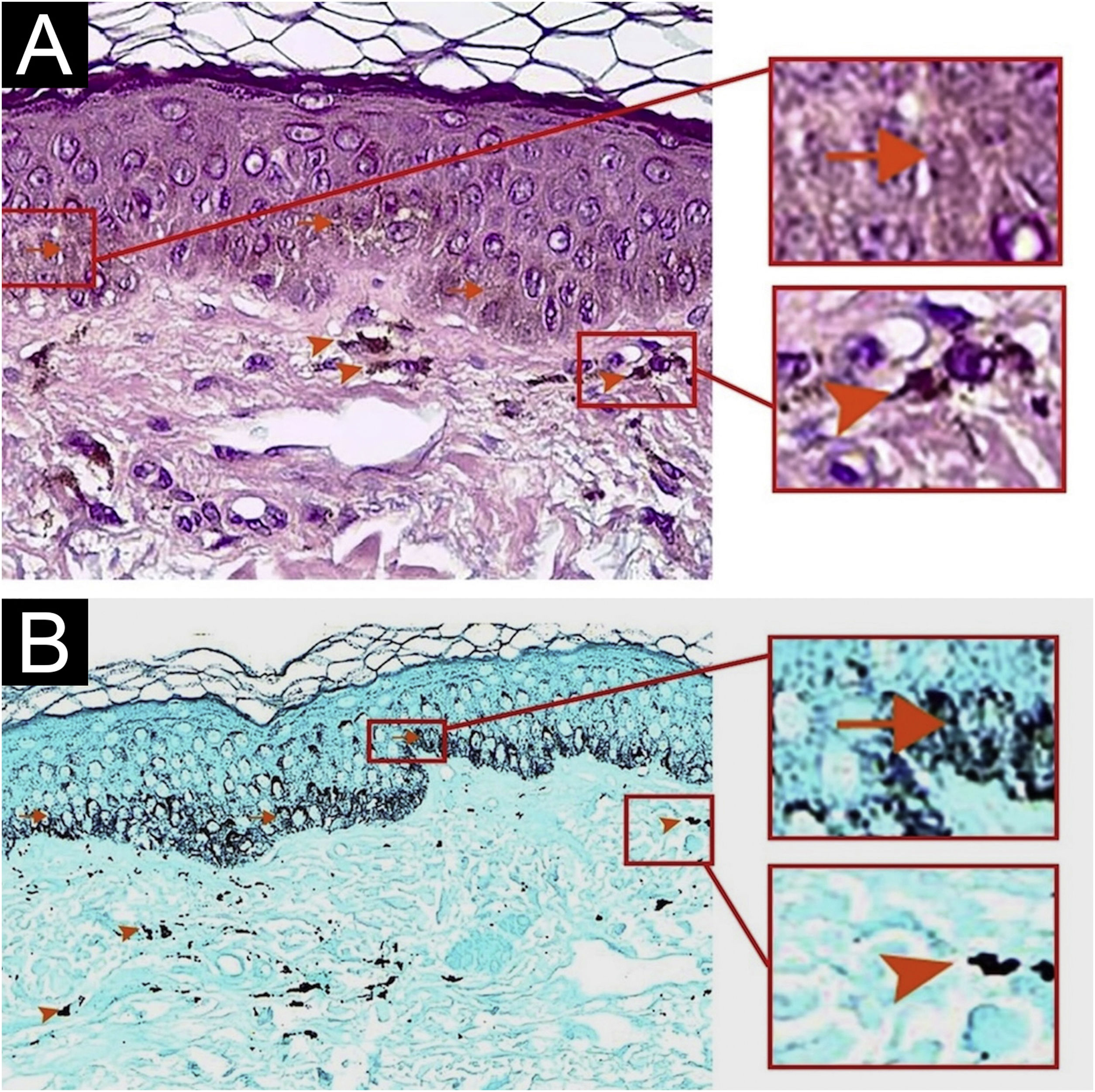
Em virtude da suspeita de fotopigmentação, um evento adverso do metimazol, foi recomendada fotoproteção. Foi solicitada biopsia da mácula de cor marrom na região bucinadora, cuja histopatologia mostrou estrato córneo normal, espessura epidérmica normal, pigmentação melânica aumentada na camada basal da epiderme e vários melanófagos na derme papilar (colorações pelo HE e método de Fontana‐Masson; fig. 2A e B). A coloração para identificação de deposição de hemossiderina foi negativa. O uso de metimazol foi interrompido e foi iniciado propiltiouracil 200mg/dia.
Histopatologia de mancha hiperpigmentada na região bucinadora revelou aumento do pigmento melanina nas células basais da epiderme (setas) e alguns melanófagos na derme superficial (pontas de seta). (A) Hematoxilina & eosina (ampliação de 100×). (B) Fontana Masson (ampliação de 100×).
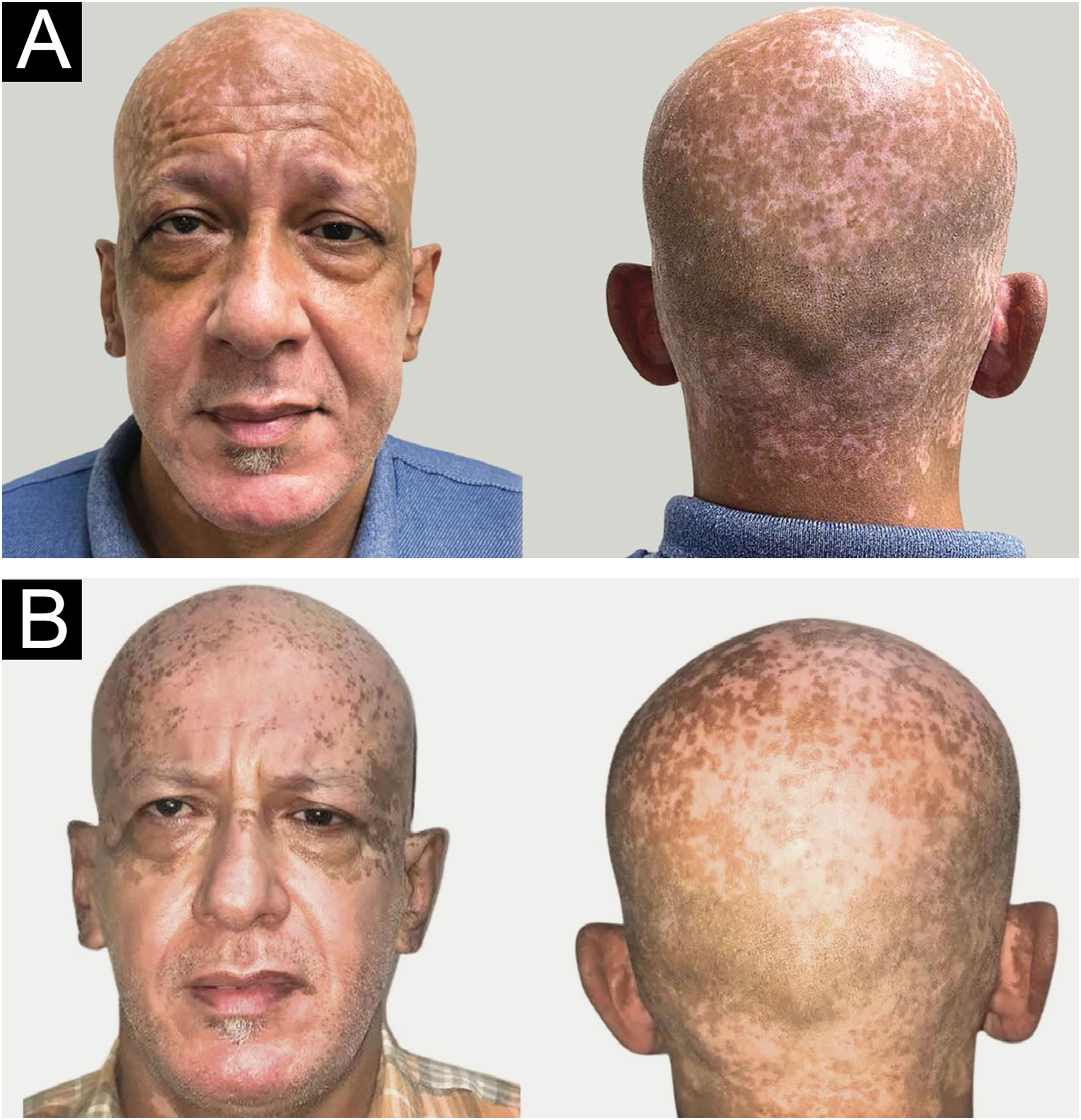
Em março de 2021, foi recomendado o uso de chapéu e protetor solar (fig. 3A). Em outubro de 2021 (TSH 0,8μIU/mL, FT4 1,64 ng/mL), houve clareamento significante nas lesões do couro cabeludo, face e pavilhões auriculares (fig. 3B) após a descontinuação do metimazol e início das medidas fotoprotetoras.
(A) Seis meses após o início do metimazol, presença de hiperpigmentação difusa acastanhada em toda a região cefálica (março de 2021). (B) Oito meses após a mudança para propiltiouracil, em associação ao uso de protetor solar e chapéu, observa‐se clareamento significante das manchas hiperpigmentadas da face (outubro de 2021).
Que seja de conhecimento dos autores, o desenvolvimento de hiperpigmentação restrita às áreas de vitiligo associado ao uso de metimazol não foi descrito anteriormente na literatura. A doença de Graves é comorbidade autoimune associada ao vitiligo, com co‐ocorrência incomum.1 A hiperpigmentação da pele, rara na doença de Graves,2 foi descrita na terapia com furosemida3 e como efeito adverso na bula do metimazol.
A hiperpigmentação induzida por medicamentos é responsável por 10% a 20% dos casos de escurecimento adquirido da cor natural da pele.4 Essa complicação geralmente é consequência de hipermelanose, aumento de cromóforos de origem não melânica ou deposição de pigmentos endógenos e exógenos.3,4 Confirmar a participação do medicamento na hiperpigmentação da pele pode ser desafiador, especialmente se a pigmentação for de início tardio ou em caso de uso concomitante de medicamentos.5
A hiperpigmentação na doença de Graves pode estar relacionada ao aumento do hormônio adrenocorticotrófico (ACTH) hipofisário para compensar a manipulação acelerada do cortisol. O ACTH e o hormônio estimulante do melanócito (MSH) têm vários aminoácidos em comum, atraindo, portanto, melanócitos residuais no vitiligo. O ACTH aumenta a ativação do receptor de melanocortina nos melanócitos. No entanto, os melanócitos epidérmicos têm receptores de TSH sensíveis aos anticorpos da doença de Graves.2
A hiperpigmentação na pele exposta ao sol após o início do uso do metimazol no caso apresentado sugere fotossensibilização induzida pelo medicamento, provavelmente relacionada à pigmentação espontânea. Que seja de conhecimento dos autores, a justificativa fisiopatológica para a pigmentação restrita às áreas de vitiligo é desconhecida. A substituição do metimazol por propiltiouracil parece melhorar a pigmentação, embora não seja possível excluir um potencial benefício adicional do filtro solar e a melhora do hipertireoidismo.
Em casos de hiperpigmentação induzida por medicamentos, a história e o exame clínico devem se concentrar na distribuição topográfica; avaliação histopatológica pode ser considerada para analisar o padrão de distribuição da melanina e processos inflamatórios associados. O diagnóstico pode ser confirmado quando há resolução dos sintomas após a interrupção do medicamento.4
Deposição de hemossiderina pode contribuir para a pigmentação no hipertireoidismo em decorrência do aumento da fragilidade capilar nessa disfunção da tireoide.6 No paciente do presente caso, a hiperpigmentação acastanhada ocorreu apenas em áreas de manchas de vitiligo anteriores expostas ao sol. A pigmentação acentuada no rosto pode estar relacionada à alta densidade de pelos velos nessa área, atuando como reservatório de melanócitos.
Os mecanismos pelos quais o metimazol leva a alterações pigmentares são mal compreendidos, merecendo investigação adicional. Embora o desenvolvimento de hiperpigmentação em áreas de vitiligo no presente caso sugira fenômeno induzido por medicamentos, não se pode excluir outros mecanismos potenciais contribuindo para essa complicação.
Suporte financeiroNenhum.
Contribuição dos autoresNicolau Lima: Concepção e o desenho do estudo; Levantamento dos dados, ou análise e interpretação dos dados; Redação do artigo ou revisão crítica do conteúdo intelectual importante; Participação efetiva na orientação da pesquisa.
Meyer Knobel: Redação do artigo ou revisão crítica do conteúdo intelectual importante.
Mayara Chinelatto: Revisão crítica da literatura.
Maria Victória Quaresma: Redação do artigo ou revisão crítica do conteúdo intelectual importante; Aprovação final da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Lima N, Knobel M, Chinelatto M, Quaresma MV. First case of hyperpigmentation in vitiligo after use of methimazole in a patient with Graves’ disease. An Bras Dermatol. 2025;100. https://doi.org/10.1016/j.abd.2024.06.006
Trabalho realizado no Departamento de Dermatologia, Hospital das Clínicas, Faculdade de Medicina, Universidade de São Paulo, São Paulo, SP, Brasil e Faculdade de Medicina, Universidade de Ribeirão Preto, Guarujá, SP, Brasil.