O curso da urticária crônica espontânea (UCE) pode ser influenciado por infecções, depressão e estresse.
ObjetivoO objetivo do estudo foi investigar o impacto da pandemia de COVID‐19 no curso da UCE refratária, juntamente com a adesão dos pacientes ao omalizumabe e ajustes no tratamento.
MétodosA escala Urticária Activity Score (UAS7) foi utilizada para avaliar a atividade da doença. As escalas Fear of COVID‐19 (FC‐19s) e Depression Anxiety Stress Scale (DASS‐21) foram utilizadas para avaliar o estado de saúde mental. Todas as escalas foram utilizadas durante o período de quarentena (PQ) e retorno ao período normal (RTPN). A escala UAS7 antes da pandemia (AP) foi registrada a partir dos prontuários dos pacientes.
ResultadosForam avaliados 104 pacientes com UCE recebendo omalizumabe. Os escores da UAS7 durante o PQ foram significativamente maiores do que os do RTPN e AP (p <0,01). Os escores da DASS‐21 e FC‐19 foram significativamente maiores durante o PQ em comparação ao RTPN (p <0,01). Dezenove (18,2%) pacientes interromperam o tratamento com omalizumabe, e nove pacientes prolongaram os intervalos entre as doses subsequentes durante a pandemia. Os escores da UAS7 no PQ foram significativamente maiores nos pacientes que interromperam o tratamento com omalizumabe do que naqueles que continuaram (p <0,001). Entre os pacientes que continuaram o tratamento com omalizumabe, 22,4% tiveram aumento da atividade da urticária e maiores escores na escala FC‐19 em comparação com aqueles com atividade de doença estável (p=0,008).
Limitações do estudoO pequeno tamanho da amostra de pacientes com intervalos prolongados de omalizumabe e a falta de avaliação da saúde mental com os mesmos instrumentos anteriores ao estudo.
ConclusãoO medo induzido pela COVID‐19 pode gerar aumento na atividade da doença. Portanto, os pacientes em uso de omalizumabe devem continuar seu tratamento, e intervalos prolongados sem omalizumabe podem ser considerados em pacientes com bom controle da urticária.
A urticária crônica espontânea (UCE) é condição debilitante que se apresenta com pápulas urticariformes, angioedema ou ambos com duração de seis semanas ou mais.1 A diretriz internacional de urticária EAACI/GA2 LEN/EDF/WAO recomenda anti‐histamínicos H1 de segunda geração como terapia de primeira linha. Um incremento de quatro vezes na dose como terapia de segunda linha pode melhorar a resposta; entretanto, alguns casos não respondem aos anti‐histamínicos. O omalizumabe é o único agente biológico aprovado para pacientes com UCE que permanecem sintomáticos apesar da dose alta de anti‐histamínico H1.1–4
A imprevisibilidade do surgimento de pápulas urticariformes ou angioedema e a natureza avassaladora da coceira podem levar ao estresse persistente e à redução da qualidade de vida. Estudos relataram associação entre estresse, ansiedade, depressão e UCE.5–7 É importante avaliar esses fatores com ferramentas validadas.
Desde que a Organização Mundial da Saúde declarou a doença do coronavírus 2019 (COVID‐19) emergência de saúde pública de interesse internacional, uma pandemia,8 diversas consequências clínicas entraram em cena. Essa doença infecciosa imprevisível e de rápida disseminação vem causando preocupação universal, mas também ansiedade e angústia.9 Como estudos anteriores elucidaram que o bem‐estar mental havia sido afetado durante os surtos da doença, é esperado que os resultados psicossomáticos adversos aumentem.10–12 O aspecto psicológico da COVID‐19 em termos de medo, estresse, ansiedade e depressão ainda não foi completamente esclarecido, especialmente em pacientes com doenças crônicas.
Após a detecção do primeiro caso de COVID‐19 na Turquia em 9 de março de 2020, várias medidas de contenção, como distanciamento social, restrições de viagem e fechamento de escolas e locais de trabalho, foram implementadas. Esse “período de quarentena (PQ)” durou três meses. À medida que o número de casos diminuiu até o final de maio de 2020, as restrições diminuíram gradualmente em um esforço para manter a rotina diária. Esse “retorno ao período normal (RTPN)” durou três meses, até o final de agosto de 2020. Os comportamentos dos pacientes com doenças crônicas foram fortemente afetados durante a pandemia, considerando sua adesão aos medicamentos e comparecimento às consultas de seguimento; entretanto, não há dados documentados demonstrando as consequências das restrições no comportamento de pacientes com doenças crônicas. Também se pode esperar que os pacientes com UCE sejam afetados de maneira semelhante pela pandemia, e é importante conhecer a influência da pandemia sobre esses pacientes, especialmente quando se considera a estreita relação entre a ativação da UCE e o estado psicológico dos pacientes. Portanto, nosso objetivo foi investigar o impacto da pandemia de COVID‐19 no curso da UCE refratária, juntamente com a adesão dos pacientes ao omalizumabe e ajustes no tratamento.
MétodosPopulação estudada e desenho do estudoUm total de 104 pacientes com UCE em tratamento com omalizumabe foram recrutados em ambulatórios de alergia para adultos de três hospitais terciários em Istambul. Os pacientes que não compareceram às consultas de seguimento, que não tomaram as injeções de omalizumabe por diversos motivos antes da pandemia de COVID‐19 e que foram diagnosticados como portadores de doenças psiquiátricas concomitantes e de neoplasias malignas não foram incluídos no estudo.
Os pacientes foram alocados em três grupos, de acordo com seus padrões de uso do omalizumabe. Assim, foram determinados os pacientes que interromperam o tratamento com omalizumabe (Grupo 1), os pacientes que estenderam o intervalo de tempo entre as injeções subsequentes de omalizumabe (Grupo 2) e os pacientes que continuaram com as injeções regulares de omalizumabe (Grupo 3) durante o período do estudo. Todos os indivíduos foram avaliados com os instrumentos do estudo no PQ e no RTPN. Além disso, os dados de atividade da urticária avaliados pelo Urticaria Activity Score (UAS7) antes da pandemia (AP) foram obtidos dos prontuários dos pacientes.
Avaliação da atividade da urticária e estado mentalA atividade da doença foi avaliada pelo UAS7, um sistema simples de pontuação relatado pelo paciente. Os pacientes avaliam a urticária pontuando a gravidade do prurido e o número de lesões de 0 a 3 em sete dias consecutivos.13
Os escores da UAS7 foram estratificados em cinco faixas de pontuação que descrevem a atividade da doença variando de livre da urticária a urticária grave.14 A mudança para uma faixa de escore de atividade da doença mais alta foi definida como “aumento da atividade da urticária”.
O estado mental dos participantes foi determinado pela versão turca da Depression‐Anxiety‐Stress Scale (DASS‐21) e da escala Fear of COVID‐19 Scale (FC‐19s).15,16
O DASS‐21 é um questionário autoaplicável de 21 itens. Os indivíduos avaliados indicam quanto as afirmações se aplicam a eles na última semana, utilizando escala Likert que varia de 0 (nunca) a 3 (na maioria das vezes, sempre).
O medo da COVID‐19 foi avaliado com a escala FC‐19s. As respostas da FC‐19s foram registradas na escala Likert de cinco pontos, variando de “discordo totalmente” (1) a “concordo totalmente” (5). O escore mais alto representou maior medo da COVID‐19.
Este estudo foi aprovado pelo Ministério da Saúde da Turquia (MST; 2020‐09‐09T12_40_50) e pelo conselho de revisão institucional e pelo Comitê de Ética do centro coordenador (2021‐96399). O consentimento informado foi obtido de todos os participantes do estudo.
Análise estatísticaA análise estatística foi realizada com a versão SPSS.25 (SPSS Inc., Armonk, NY, EUA). As variáveis categóricas foram resumidas como frequências e porcentagens. As variáveis contínuas foram dadas como média e desvio padrão ou mediana (IIQ 25‐75). O teste de Wilcoxon foi usado para comparação de dados que não apresentavam distribuição normal. O teste U de Mann‐Whitney e o teste de Kruskal‐Wallis foram realizados para avaliar os diferentes grupos. A relação entre os escores da UAS7, DASS‐21 e FC‐19s foi analisada pelo teste de correlação de Spearman. O valor de p bilateral <0,05 determinou a significância estatística. O software GraphPad Prism foi utilizado para análise gráfica.
ResultadosCaracterísticas clínicas e demográficas dos pacientes com UCEForam incluídos no estudo 104 pacientes. A média de idade foi de 42,74±12 anos, e a maioria (74%) dos pacientes era do sexo feminino. A duração média da UCE era de quatro anos (IIQ 25‐75: 3‐8,75), e a duração média do tratamento com omalizumabe foi de 24 meses (IIQ 25‐75: 14‐36,75). Cinquenta (48,1%) pacientes apresentavam urticária crônica induzida concomitante, como mostrado em detalhes na tabela 1. O estresse foi o fator desencadeante mais comum (51,9%), enquanto infecções foram o fator desencadeante em 7,7% dos pacientes. As características demográficas e clínicas dos 104 pacientes com UCE são mostradas na tabela 1.
Características demográficas e clínicas de 104 pacientes
| Idade, média anos±DP | 42,74±12 |
| Sexo, n (%) | |
| Feminino | 77 (74) |
| Masculino | 27 (26) |
| Doença concomitante, n (%) | 46 (44,2) |
| Doenças cardiovasculares | 4 (3,8) |
| Doenças respiratórias | 10 (9,6) |
| Doenças da tireoide | 10 (9,6) |
| Hipertensão | 10 (9,6) |
| Arritmia | 2 (1,9) |
| Diabetes mellitus | 13 (12,5) |
| Hiperlipidemia | 6 (5,8) |
| Outras | 8 (7,7) |
| Duração da urticária, anos, mediana (IIQ 25‐75) | 4 (3‐8,75) |
| Duração do uso de omalizumabe, meses, mediana (IIQ 25‐75) | 24 (14‐36,75) |
| Presença de angioedema, n (%) | 66 (63,5) |
| Presença de urticária induzida, n (%) | 50 (48,1) |
| Urticária ao frio | 13 (12,5) |
| Urticária solar | 31 (29,8) |
| Urticária aquagênica | 3 (2,9) |
| Urticária de pressão tardia | 18 (17,3) |
| Urticária vibratória | 1 (1) |
| Urticária colinérgica | 13 (12,5) |
| Urticária de contato | 3 (2,9) |
| Dermografismo | 23 (22,1) |
| Presença de fatores desencadeantes, n (%) | 68 (65,4) |
| Medicamentos | 22 (21,2) |
| Alimentos | 31 (29,8) |
| Estresse | 54 (51,9) |
| Infecção | 8 (7,7) |
| Outros | 7 (6,7) |
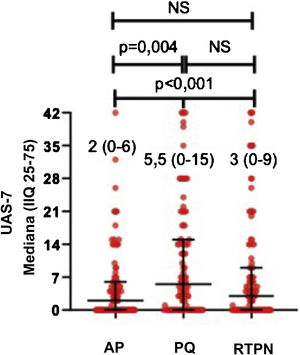
Os escores da UAS7 em todos os pacientes durante o PQ (UAS7PQ) foram significativamente maiores do que os determinados no RTPN (UAS7RTPN) e antes da pandemia (UAS7AP; p <0,01) Na análise post hoc, a mediana da UAS7PQ foi maior do que os valores determinados antes da pandemia (UAS7AP; p=0,004), enquanto os escores medianos da UAS7 foram semelhantes entre o PQ e o RTPN (UAS7RTPN; fig. 1).
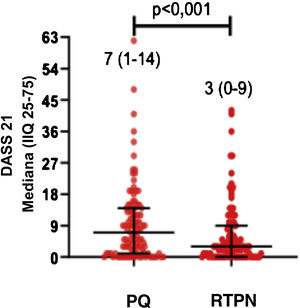
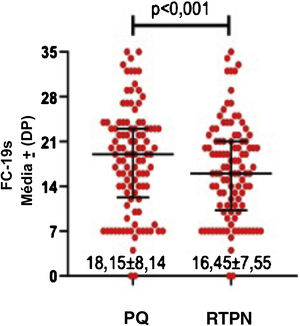
Os escores da DASS‐21 e FC‐19s foram significativamente maiores durante o PQ em comparação ao RTPN (p <0,01; figs. 2 e 3).
O sexo feminino apresentou escores significativamente maiores na FC‐19s (p=0,024) durante o PQ, enquanto os escores na UAS7 e DASS‐21 não diferiram entre os sexos. Os escores na UAS7, DASS‐21, FC‐19s não diferiram em relação a idade, escolaridade, presença de angioedema ou doença crônica durante os dois períodos (tabela 2).
UAS7, DASS‐21s, FC‐19s dos pacientes de acordo com características demográficas e clínicas
| UAS7 mediana (IIQ: 25‐75) | FC‐19 (média±DP) | DASS‐21t mediana (IIQ: 25‐75) | |||||
|---|---|---|---|---|---|---|---|
| AP | PQ | RTPN | PQ | RTPN | PQ | RTPN | |
| Sexo | |||||||
| Feminino | 2 (0‐5,5) | 5 (0‐18) | 3 (0‐12) | 19,25±7,93 | 17,31±7,19 | 7 (2,5‐14,5) | 3 (1‐9) |
| Masculino | 3 (0‐8) | 6 (0‐12) | 4 (0‐9) | 15,04±8,07 | 14±8,15 | 6 (0‐14) | 1 (0‐9) |
| p | NS | NS | NS | 0,024 | NS | NS | NS |
| Idade | |||||||
| 18‐40 | 2 (0‐5,25) | 4,5 (0‐14,25) | 3 (0‐7,5) | 18,45±7,66 | 16,64±6,49 | 8 (1‐14) | 3 (0‐10,5) |
| 40‐65 | 4 (0‐8,5) | 7 (0‐19,5) | 4 (0‐12,5) | 18,34±8,52 | 16,7±8,29 | 7 (1,5‐13,5) | 3 (1‐9) |
| > 65 | 0 (0‐0) | 0 (0‐21) | 0 (0‐15) | 14±5,09 | 11,5±3,11 | 3,5 (0‐9,25) | 3 (0‐9) |
| p | NS | NS | NS | NS | NS | NS | NS |
| Presença de angioedema | 2 (0‐6) | 5 (0‐15) | 3 (0‐7,5) | 18,94±8,13 | 17,09±7,66 | 9 (3‐14,25) | 3,5 (1‐10) |
| p | NS | NS | NS | NS | NS | NS | NS |
| Presença de doenças crônicas | 1 (0‐7) | 10,5 (0‐21,75) | 4,5 (0‐14) | 18,67±8,44 | 16,67±8,02 | 6 (1‐11) | 3 (0‐8,25) |
| p | NS | NS | NS | NS | NS | NS | NS |
UAS7, Urticaria Activity Score somado ao longo de 7 dias; DASS‐21, Depression Anxiety and Stress Scale; FC‐19s, Fear of COVID‐19 scale; IIQ, intervalo interquartil; DP, desvio padrão; AP, antes da pandemia; PQ, período de quarentena; RTPN, returno ao período normal; NS, não significativo.
Os escores na UAS7 e FC‐19s foram correlacionados entre si durante o PQ e RTPN (p=0,02, R=0,228; p=0,02, R=0,227, respectivamente; fig. 4), enquanto os escores na UAS7 não foram correlacionados com os escores na DASS‐ 21 (fig. 5 A‐B).
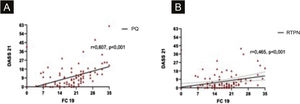
A DASS‐21 e FCV‐19S foram correlacionadas entre si durante o PQ e RTPN (p <0,001, R=0,607; p=0,02, R=0,465, respectivamente; fig. 6 A‐B).
Determinação dos grupos de estudo de acordo com a aplicação de omalizumabe durante a pandemiaSetenta e seis pacientes receberam injeções de omalizumabe com os mesmos intervalos entre as doses (Grupo 3). Os intervalos entre as injeções foram prolongados em nove pacientes (Grupo 2), e 19 (18,3%) pacientes interromperam o uso de omalizumabe (Grupo 1). O motivo do prolongamento dos intervalos de omalizumabe foi o medo da COVID‐19, enquanto os motivos mais comuns para a interrupção do tratamento com omalizumabe foram o medo do COVID‐19 e a dificuldade de comparecer aos hospitais. Alguns pacientes apresentaram mais de um motivo para a interrupção do tratamento com omalizumabe durante o PQ (tabela 3). Um total de 20% dos pacientes do Grupo 3 tiveram suas injeções em outro centro, diferente do seu centro inicial; 2,4% fizeram terapia domiciliar, e os demais continuaram em seu centro de tratamento inicial durante o período do estudo. No Grupo 2, a duração média dos intervalos entre as doses de omalizumabe foi de oito semanas (IIQ 25‐75: 6‐8). No Grupo 1, a duração mediana da interrupção do tratamento com omalizumabe foi de 16 semanas (IIQ 25‐75: 14‐19).
Respostas sobre os motivos da interrupção do uso de omalizumabe durante o período de quarentena dos pacientes
| Número de pacientes (%) | |
|---|---|
| Não fui a uma instituição de saúde por medo da COVID‐19 | 12 (63,1) |
| Tive dificuldade em conseguir consulta e/ou transporte para ir aos hospitais | 6 (31,5) |
| Não conhecia a facilitação do acesso aos medicamentos prescritos durante a pandemia | 5 (26,3) |
Os pacientes do Grupo 3 apresentaram média de UAS7AP maior do que os do Grupo 1 ou do Grupo 2 (p=0,021). A análise post hoc revelou que a mediana da UAS7AP foi maior no Grupo 3 do que no Grupo 2 (p=0,015), enquanto a mediana da UAS7AP foi semelhante entre os pacientes do Grupo 3 e os do Grupo 1 (tabela 4).
Escores de UAS7, DASS‐21s, e FC‐19s de três grupos de pacientes AP, no PQ e no RTPN
| Grupo 1 (19 pacientes) | Grupo 2 (9 pacientes) | Grupo 3 (76 pacientes) | p | ||
|---|---|---|---|---|---|
| UAS‐7 mediana (IIQ: 25‐75) | AP | 0 (0‐6) | 0 (0‐1) | 3 (0‐7) | 0,021 |
| PQ | 28 (12‐39) | 0 (0‐6,5) | 4 (0‐14) | <0,001 | |
| RTPN | 0 (0‐26) | 1 (0‐21) | 4 (0‐9) | NS | |
| FC‐19s (média±DP) | PQ | 19,42±6,69 | 16,89±9,29 | 17,99±8,4 | NS |
| RTPN | 16,47±6,12 | 14,78±7,44 | 16,64±7 | NS | |
| DASS‐21s mediana (IIQ: 25‐75) | PQ | 9 (0‐15) | 6 (0,5‐12,5) | 5,5(1‐14) | NS |
| RTPN | 4 (0‐12) | 2 (0‐4,5) | 3 (0‐9) | NS |
UAS‐7, Urticaria Activity Score somado ao longo de 7 dias; FC‐19s, Fear of COVID‐19 scale; DASS‐21, Depression Anxiety and Stress Scale; IIQ, intervalo interquartil; DP, desvio‐padrão; AP, antes da pandemia; PQ, período de quarentena; RTPN, retorno ao período normal; NS, não significante.
No PQ, a mediana da UAS7 foi diferente entre os três grupos (p <0,001). Na análise post‐hoc, a mediana da UAS7PQ foi maior nos pacientes do Grupo 1 (p <0,001), enquanto a mediana da UAS7QP foi semelhante entre os pacientes do Grupo 2 e os do Grupo 3 (p> 0,05; tabela 4).
Nos três grupos, a mediana da UAS7QP foi maior que a mediana da UAS7AP, e esse aumento foi estatisticamente significativo nos pacientes do Grupo 1 (p <0,001) e naqueles do Grupo 3 (p=0,008).
Os escores da FC‐19s e DASS‐21 não diferiram entre os três grupos no PQ (tabela 4).
No RTPN, observou‐se que todos os pacientes do Grupo 1 reiniciaram o omalizumabe devido à piora dos sintomas. As medianas dos escores da UAS7, FC‐19s e DASS‐21 não foram diferentes entre os três grupos no RTPN (tabela 4).
Escores na FC‐19s em pacientes com aumento da atividade da urticária durante o PQTrinta e quatro (32,7%) pacientes apresentaram aumento da atividade da urticária durante o PQ. Entre esses pacientes, os escores da FC‐19s durante o PQ e ter comorbidades associadas a COVID‐19 mais grave foram estatisticamente maiores do que naqueles com atividade de urticária estável (p=0,013 e p=0,03, respectivamente). Um total de 22,4% dos pacientes do Grupo 3 tiveram aumento da atividade da urticária durante o PQ, e esses pacientes apresentaram escores de FC‐19s mais altos em comparação com aqueles com atividade de doença estável (p=0,008).
DiscussãoEste é o primeiro estudo que investiga o impacto da pandemia de COVID‐19 em pacientes com UCE refratária tratados com omalizumabe. Os achados do presente estudo revelaram que a pandemia de COVID‐19 pode prejudicar o curso da UCE refratária e as intervenções para apoiar os tratamentos em andamento são, portanto, cruciais. Além disso, ele fornece contribuição adicional às recomendações da recente declaração da European Academy of Allergy and Clinical Immunology (EAACI) sobre tratamento com biológicos na UCE durante a pandemia,17 mostrando que até oito semanas de intervalo entre injeções subsequentes de omalizumabe podem ser toleradas na UCE refratária durante a pandemia.
Os pacientes com UCE apresentam níveis mais altos de estresse, e a atividade da doença está correlacionada com os níveis de estresse emocional.18,19 Estudo recente avaliou o impacto da pandemia em 509 pacientes com UCE leve/moderada e revelou aumento da atividade da urticária e níveis mais altos de estresse durante o PQ em comparação com AP e RTPN.20 No presente estudo foi possível determinar o aumento da atividade da doença em pacientes com UCE refratária que receberam omalizumabe durante a pandemia. Como os distúrbios emocionais e os eventos estressantes da vida influenciam o curso da UCE, pode‐se especular que a pandemia de COVID‐19 teria efeitos prejudiciais nos pacientes com UCE.
O medo é uma das características das doenças infecciosas.21 Com a alta taxa de infecção e mortalidade relativamente alta, os indivíduos podem se preocupar com a COVID‐19. A esse respeito, utilizou‐se a escala FC‐19s, que é ferramenta válida para avaliar o medo da COVID‐19 e está correlacionada significativamente com depressão e ansiedade.16 Shin et al.22 também afirmaram que o neurocircuito do medo/ansiedade tem sobreposição e interação com o neurocircuito que orquestra a resposta ao estresse. No presente estudo, os escores da FC‐19s foram significativamente maiores durante o PQ em comparação ao RTPN, e os escores da FC‐19s foram correlacionados com os escores da escala DASS‐21. Além disso, entre os pacientes que continuaram o tratamento com omalizumabe, aqueles que apresentaram aumento da atividade da urticária apresentaram escores mais altos de FC‐19s no PQ, indicando o impacto do medo no curso da UCE.
A resposta a um fator de estresse psicossocial é diferente entre os sexos. A redução do condicionamento do medo é observada em homens estressados, enquanto as mulheres estressadas podem mostrar reconhecimento aumentado do medo.23,24 Essa pode ser a provável explicação para o fato de as pacientes do sexo feminino apresentarem escores de FC‐19s mais altos, enquanto os escores na escala DASS‐21 não foram diferentes dos observados nos homens.
As medidas de contenção, como redução de visitas a hospitais e isolamento domiciliar implementadas para evitar a propagação dessa doença altamente contagiosa, tornaram‐se obstáculo para o seguimento e tratamento de doenças crônicas. De maneira similar, Kocatürk et al. afirmaram que o número semanal de pacientes de urticária crônica (UC) tratados nos centros UCARE diminuiu mais de 50% durante a pandemia de COVID‐19.25
Estudo avaliando os efeitos da pandemia em pacientes com UC revelou 44% de interrupção do tratamento com omalizumabe.26 No presente estudo, 81,7% dos pacientes continuaram com omalizumabe. Essa taxa de adesão relativamente mais alta pode ser atribuída aos regulamentos nas clínicas do presente estudo para a continuação dos tratamentos em andamento com omalizumabe durante a pandemia.
O omalizumabe só pode ser injetado em hospitais mediante receita médica na Turquia. Durante o PQ, o MST facilitou o acesso à medicação prescrita para aqueles que tinham relatórios de consentimento de prescrição válidos. Pela facilitação do acesso à medicação prescrita, 20% dos pacientes do presente estudo continuaram suas injeções em diferentes centros além do centro de saúde inicial, enquanto 2,4% dos pacientes fizeram terapia domiciliar. Nesse ponto, deve‐se enfatizar a importância da atenção específica para intervenções personalizadas em relação a medicamentos utilizados em doenças crônicas durante períodos especiais, como surtos de doenças, a fim de manter o acompanhamento e o tratamento efetivos. Em estudo recente de Öztürk et al., eles afirmaram que 59% dos alergistas de adultos/pediátricos na Turquia utilizavam a telemedicina para o tratamento de pacientes com urticária/angioedema.27
A recente declaração da EAACI sobre o uso de produtos biológicos durante a COVID‐19 aconselhou a não alterar a terapia em indivíduos não infectados com base na opinião de especialistas.17 Entretanto, ajustes bem‐sucedidos no tratamento com omalizumabe foram demonstrados em pacientes com UCE refratária antes da pandemia.28–30 No presente estudo, foi demonstrado pela primeira vez que os ajustes de intervalo entre doses podem ser tolerados em pacientes com UCE refratária durante a pandemia, mas a interrupção pode piorar o curso da doença. Os pacientes com intervalos prolongados entre doses de omalizumabe apresentaram escores mais altos na UAS7AP. Portanto, o prolongamento do intervalo pode ser recomendado para pacientes com bom controle da urticária, a fim de reduzir as visitas hospitalares durante a pandemia.
Por outro lado, 78,9% dos pacientes que interromperam o uso de omalizumabe apresentaram aumento da atividade da urticária. Como os pacientes do presente estudo tinham UCE refratária, era esperada a perda do controle da doença quando o omalizumabe foi interrompido.
A COVID‐19 tem sido um risco para todos os seres humanos, e comorbidades como diabetes mellitus, hipertensão, doenças cardiovasculares e doenças respiratórias crônicas foram identificadas como fatores de risco para COVID‐19 grave. No presente estudo, os pacientes com essas comorbidades apresentaram maiores escores nas escalas UAS7, DASS‐21, FC‐19s, mas não foram estatisticamente significativos. Apesar disso, 47,1% deles tiveram aumento de atividade da urticária durante o PQ, e isso é estatisticamente significativo quando comparados aos pacientes sem comorbidades. Pode‐se especular que o conhecimento de ter comorbidades que são associadas à infecção grave por COVID‐19 resultou na perda do controle da doença, o que pode ser outro indicador da associação de medo e estresse com atividade de urticária.
Houve duas limitações no presente estudo. A primeira é o pequeno tamanho da amostra de pacientes com intervalos prolongados entre doses de omalizumabe, o que pode ter afetado a acurácia dos resultados estatísticos. Recomenda‐se aos pacientes que não alterem a terapia, de acordo com a declaração da EAACI.17 Os pacientes do Grupo 2 prolongaram os intervalos independentemente das sugestões médicas.
Como segunda limitação, não foi possível avaliar a saúde mental dos pacientes com as mesmas ferramentas anteriores ao estudo.
ConclusãoFoi observado que tanto o medo quanto o estresse induzidos pela COVID‐19 e a interrupção do tratamento com omalizumabe produziram aumento na atividade da urticária. Portanto, os pacientes recebendo omalizumabe devem continuar seu tratamento com os mesmos intervalos de dose ou intervalos prolongados; intervenções personalizadas, como telemedicina e terapia domiciliar, devem ser consideradas para pacientes com doenças crônicas durante períodos de surtos de doenças, a fim de manter acompanhamento eficaz e reduzir visitas desnecessárias aos hospitais.
Suporte financeiroNenhum.
Contribuição dos autoresMüge Olgaç: Fez contribuições substanciais para concepção e planejamento, obtenção dos dados, análise e interpretação dos dados; participou na redação do manuscrito, e revisão crítica do conteúdo intelectual importante.
Osman Ozan Yeğit: Fez contribuições substanciais na obtenção de dados, análise e interpretação dos dados; participou na redação do manuscrito, e revisão crítica do conteúdo intelectual importante.
Sengul Beyaz: Fez contribuições substanciais para a obtenção dos dados, análise e interpretação dos dados; participou da redação do manuscrito.
Özdemir Can Tüzer: Fez contribuições substanciais para a obtenção dos dados, análise e interpretação dos dados; participou da redação do manuscrito.
Deniz Eyice Karabacak: Fez contribuições substanciais para a concepção e planejamento, obtenção dos dados, participou na redação do manuscrito.
Nida Oztop: Fez contribuições substanciais para a obtenção dos dados, análise e interpretação dos dados; participou da redação do manuscrito.
Pelin Karadağ: Fez contribuições substanciais para a obtenção dos dados, interpretação dos dados; participou da redação do manuscrito.
Raif Coşkun: Fez contribuições substanciais para concepção e planejamento, obtenção dos dados ou análise e interpretação dos dados; participou da redação do manuscrito.
Semra Demir: Fez contribuições substanciais para concepção e planejamento, obtenção dos dados, análise e interpretação dos dados; participou na redação do manuscrito e na revisão crítica do conteúdo intelectual importante.
Bahauddin Colakoglu: Fez contribuições substanciais para concepção e planejamento, obtenção dos dados, análise e interpretação dos dados; participou na redação do manuscrito ou na revisão crítica do conteúdo intelectual importante.
Suna Buyukozturk: Fez contribuições substanciais para concepção e planejamento, aquisição dos dados, análise e interpretação dos dados; participou na revisão crítica do manuscrito para conteúdo intelectual importante.
Aslı Gelincik: Fez contribuições substanciais para concepção e planejamento, aquisição dos dados, análise e interpretação dos dados; participou na revisão crítica do manuscrito para o conteúdo intelectual importante.
Conflito de interessesNenhum.
Como citar este artigo: Olgaç M, Yeğit OO, Beyaz Ş, Öztop N, Tüzer C, Eyice D, et al. Impact of COVID‐19 pandemic on the course of refractory chronic spontaneous urticaria under omalizumab treatment. An Bras Dermatol. 2023;98:189–97.
Trabalho realizado na Divisão de Imunologia e Doenças Alérgicas, Şişli Hamidiye Etfal Research and Education Hospital; Divisão de Imunologia e Doenças Alérgicas, Departamento de Clínica Médica, Faculdade de Medicine de Istambul, Istanbul University, e Divisão de Imunologia e Doenças Alérgicas, Okmeydanı Research and Education Hospital, Istambul, Turquia.